
【题目】己知:铝热反应是放热反应,又知,常温下:
4Al(s)+3O2(g)= 2Al2O3(s) ΔH1
4Fe(s)+3O2(g)=2Fe2O3(s) ΔH2
下面关于ΔH1、ΔH2的比较正确的是
A.ΔH1>ΔH2 B.ΔH1<ΔH2 C.ΔH1=ΔH2 D.无法计算
科目:高中化学 来源: 题型:
【题目】在下列条件下,两种气体的分子数一定相等的是
A.同密度、同压强的 N2 和 C2H4 B.同体积、同密度的C2H4和CO
C.同温度、同体积的 O2和N2 D.同压强、同体积的 O2和 N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应:2NO(g)+O2(g)![]() 2NO2(g),在体积不变的密闭容器中反应,一定达到平衡状态的标志是( )
2NO2(g),在体积不变的密闭容器中反应,一定达到平衡状态的标志是( )
A.单位时间内生成n mol O2的同时生成n mol NO2
B.混合气体的颜色不再改变的状态
C.ν(NO2):ν(NO):ν(O2)=2:2:1的状态
D.混合气体的密度不再改变的状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲烷中混有乙烯,欲除乙烯得到纯净的甲烷,可依次将其通过下列哪组试的洗气瓶( )
A.澄清石灰水,浓H2SO4
B.溴水,浓H2SO4
C.酸性高锰酸钾溶液,浓H2SO4
D.浓H2SO4 , 酸性高锰酸钾溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图装置,完成很多电化学实验.下列有关此装置的叙述中,正确的是

A.若X为锌棒,Y为NaCl溶液,开关K置于M处,可减缓铁的腐蚀,这种方法称为牺牲阴极保护法
B.若X为碳棒,Y为NaCl溶液,开关K置于N处,可加快铁的腐蚀
C.若X为铜棒,Y为硫酸铜溶液,开关K置于M处,铜棒质量将增加,此时外电路中的电子向铜电极移动
D.若X为铜棒,Y为硫酸铜溶液,开关K置于N处,可用于铁表面镀铜,溶液中铜离子浓度将减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向0.1 mol·L-1 CH3COOH溶液中加少量水,下列有关说法错误的是( )
A.溶液中所有离子的浓度都减小
B.CH3COOH的电离程度变大
C.水的电离程度变大
D.溶液的pH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修3:物质结构与性质]磷存在于人体所有细胞中,是维持骨骼和牙齿的必要物质,几乎参与所有生理上的化学反应。回答下列问题:
(1)基态P原子的核外电子排布式为 ________,有________个未成对电子。
(2)磷的一种同素异形体——白磷(P4)的立体构型为________,其键角为__________,推测其在CS2中的溶解度________(填“大于”或“小于”)在水中的溶解度。
(3)两种三角锥形气态氢化物膦(PH3)和氨(NH3)的键角分别为93.6和107,试分析PH3的键角小于NH3的原因 ______________________________。
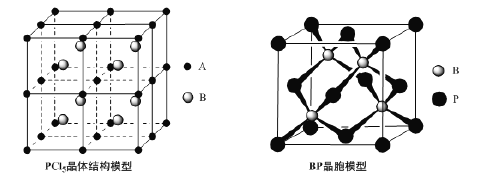
(4)常温下PCl5是一种白色晶体,其立方晶系晶体结构模型如上左图所示,由A、B两种微粒构成。将其加热至148℃熔化,形成一种能导电的熔体。已知A、B两种微粒分别与CCl4、SF6互为等电子体,则A为______,其中心原子杂化轨道类型为__________,B为________。
(5)磷化硼(BP)是一种超硬耐磨涂层材料,上右图为其立方晶胞,其中的每个原子均满足8电子稳定结构,试判断其熔点 __________(填“高于”或“低于”)金刚石熔点。
已知其B—P键长均为x cm,则其密度为 ________g﹒cm—3(列出计算式即可)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com