
| A.B的转化率为20% |
| B.m值为1 |
| C.5min内用A表示的平均反应速率为0.1mol?L-1?min-1 |
| D.平衡时反应混合物总物质的量为1mol |
| 0.2mol |
| 0.5mol |
| ||
| 5min |


科目:高中化学 来源:不详 题型:单选题
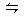 MgCl2+2Rb(g)。对于此反应的进行能给予正确解释的是( )。
MgCl2+2Rb(g)。对于此反应的进行能给予正确解释的是( )。| A.铷的金属活动性不如镁强,镁可置换出铷 |
| B.铷的沸点比镁低,把铷蒸气抽出时,平衡向右移 |
| C.铷的单质状态较化合态更稳定 |
| D.MgCl2的热稳定性不如RbCl强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 催化剂 |
| 高温高压 |
| 4 |
| 5 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用物质A表示的反应速率为0.6mol(L?s)-1 |
| B.用物质B表示的反应速率为0.3mol(L?s)-1 |
| C.2s时物质A的转化率为30% |
| D.2s时物质B的浓度为0.3mol?L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.A、B的转化率均为20% |
| B.m值为1 |
| C.5min内用A表示的平均反应速率为0.1mol?L-1?min-1 |
| D.平衡时混合物总物质的量为1mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.92.4>Ql>2Q2 | B.92.4=Q1<2Q2 |
| C.Q1=2Q2=92.4 | D.Q1=2Q2<92.4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.物质C的质量分数增加 | B.物质A的转化率增加 |
| C.平衡向逆反应方向移动 | D.m>2n |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com