
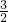 =0.36mol,此时溶液中Fe2+与Cu2+物质的量之比为0.36mol:0.24mol=3:2,实际溶液中Fe2+与Cu2+物质的量之比为2:1,这说明溶液中铁单质也和铜离子反应Fe+Cu2+=Fe2++Cu,此时溶液中溶质为硫酸亚铁与硫酸铜,根据电荷守恒n(Fe2+)+n(Cu2+)=n(SO42-),溶液中n(SO42-)=0.2L×0.6mol/L×3+0.2L×1.2mol/L=0.6mol,Fe2+与Cu2+物质的量之比为2:1,故n(Fe2+)+
=0.36mol,此时溶液中Fe2+与Cu2+物质的量之比为0.36mol:0.24mol=3:2,实际溶液中Fe2+与Cu2+物质的量之比为2:1,这说明溶液中铁单质也和铜离子反应Fe+Cu2+=Fe2++Cu,此时溶液中溶质为硫酸亚铁与硫酸铜,根据电荷守恒n(Fe2+)+n(Cu2+)=n(SO42-),溶液中n(SO42-)=0.2L×0.6mol/L×3+0.2L×1.2mol/L=0.6mol,Fe2+与Cu2+物质的量之比为2:1,故n(Fe2+)+ n(Fe2+)=n(SO42-)=0.6mol,所以n(Fe2+)=0.4mol,根据铁元素守恒,加入铁粉的物质的量n(Fe)=n(Fe2+)-n(Fe3+)=0.4mol-0.24ml=0.16mol,
n(Fe2+)=n(SO42-)=0.6mol,所以n(Fe2+)=0.4mol,根据铁元素守恒,加入铁粉的物质的量n(Fe)=n(Fe2+)-n(Fe3+)=0.4mol-0.24ml=0.16mol,

科目:高中化学 来源: 题型:填空题
| 沉淀物 | 开始沉淀时的pH | 沉淀完全时的pH |
| Mg(OH)2 | 9.6 | 11.1 |
| Fe(OH)3 | 2.7 | 3.7 |
| 实验操作 | 预期现象和结论 |
| 步骤1: | ________ |
| 步骤2: | ________ |
| 步骤3: | ________ |
| … |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com