
下列化学反应中,不属于离子反应的是( )
A.在水溶液中:CH3COOH+NH3·H2O===CH3COONH4+H2O
B.在水溶液中:Cu(OH)2+2HNO3===Cu(NO3)2+2H2O
C.Fe2O3+3CO 2Fe+3CO2
2Fe+3CO2
D.在水溶液中:CaSO4+Na2CO3===CaCO3↓+Na2SO4
科目:高中化学 来源: 题型:
实验室可以采用如图所示装置来测定某种氨基酸的分子式。取w g该种氨基酸样品,放在纯氧中充分燃烧,生成CO2、H2O和N2。请回答有关问题:
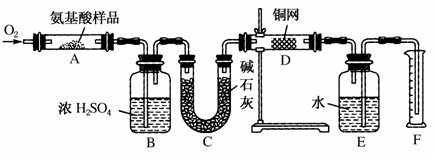
(1)E装置的作用是________________________________________________________________________。
(2)需要加热的装置是________(填字母代号)。
(3)装置D的作用是________________________________________________________________________。
(4)F处读数时应该注意:________________________________________________________________________,________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,在容积固定的V L密闭容器中加入n mol A、2n mol B,发生反应:A(g)+2B(g)2C(g) ΔH<0,反应达平衡后测得平衡常数为K,此时A的转化率为x。
(1)一段时间后上述反应达到平衡。则下列说法中正确的是________(填字母)。
A.物质A、B的转化率之比为1∶2
B.起始时刻和达到平衡后容器中的压强之比为3n∶(3n-nx)
C.当2v正(A)=v逆(B)时,反应一定达到平衡状态
D.充入惰性气体(如Ar),平衡向正反应方向移动
(2)K和x的关系满足K=__________。在保证A浓度不变的情况下,扩大容器的体积,平衡______(填字母)。
A.向正反应方向移动
B.向逆反应方向移动
C.不移动
(3)该反应的逆反应速率与时间的关系如图所示。
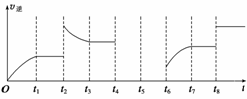
①由图可知,反应在t1、t3、t7时都达到了平衡,而t2、t8时都改变了一种条件,试判断改变的条件:
t2时________________________________________________________________________;
t8时________________________________________________________________________。
②t2时平衡向______(填“正反应”或“逆反应”)方向移动。
③若t4时降压,t5时达到平衡,t6时增大反应物的浓度,请在图中画出t4~t6时逆反应速率与时间的关系线。
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D是中学常见的混合物分离或提纯的基本装置。
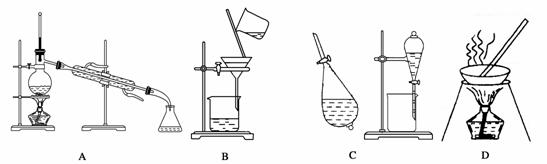
请根据混合物分离或提纯的原理,回答在下列实验中需要使用哪种装置。将A、B、C、D填入适当的空格中。
(1)除去Ca(OH)2溶液中悬浮的CaCO3__________________________________________;
(2)从碘水中提取碘__________________________________________;
(3)用自来水制取蒸馏水___________________________________;
(4)分离植物油和水_______________________________________;
(5)除去粗盐中的泥沙__________________________________________;
(6)与海水晒盐原理相符的是__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在无土栽培中,配制一定量的营养液,使其中含有50 mol NH4Cl、16 mol KCl和24 mol K2SO4,若改用KCl、NH4Cl、(NH4)2SO4三种固体为原料配制,三者的物质的量依次是(单位为mol)( )
A.2、64、24 B.64、2、24 C.30、50、12 D.16、50、24
查看答案和解析>>
科目:高中化学 来源: 题型:
进行下面的实验要用到下列一种或几种仪器,请用这些仪器的名称填空。
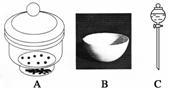
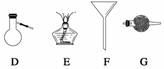
(1)欲干燥NH3需使用仪器________________________________________________;
(2)欲分离互不相溶的两种液体,可使用____________________________________;
(3)欲分离液态混合物中沸点不同的组分,可使用_____________________________;
(4)欲分离悬浮于液体中的固体物质,可使用_________________________________;
(5)欲用胆矾晶体(CuSO4·5H2O)制无水硫酸铜固体,可使用:___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
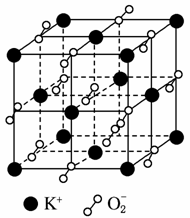
高温下超氧化钾晶体呈立方体结构,晶体中氧的化合价部分为0价,部分为-2价。如右图所示为超氧化钾晶体的一个晶胞(晶体中最小的重复单元),则下列说法中正确的是( )
A.超氧化钾的化学式为KO2,每个晶胞含有4个K+和4个O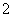
B.晶体中每个K+周围有8个O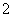 ,每个O
,每个O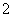 周围有8个K+
周围有8个K+
C.晶体中与每个K+距离最近的K+有8个
D.晶体中,0价氧与-2价氧的数目比为2:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com