
有关甲烷,甲醇,甲醚,甲醛,甲酸的叙述:
①1mol甲烷与等物质量的Cl2在光照条件下反应生成lmool一氯甲烷
②能够与金属钠反应的有甲醇和甲酸
③O.1 mol上述各有机物的混合物充分燃烧,生成标准状况下的CO2 2.24 L
④以上五种有机物,能够在一定条件下发生银镜反应的仅有甲醛
⑤常温常压下,甲烷、甲醛呈气态
⑥l50℃时,各有机物分别在足量氧气中充分燃烧,维持原来的温度和压强,
烷燃烧前后体积不变下列组合正确的是
A.②③⑤ B.②⑤⑥ C.②④⑤ D.①③⑤
科目:高中化学 来源: 题型:
①-OH ②OH- ③-Br ④NO2 ⑤ ⑥-C6H5 ⑦Br- ⑧-COOH ⑨-CH3其中不是官能团的是
⑥-C6H5 ⑦Br- ⑧-COOH ⑨-CH3其中不是官能团的是
A.①③④⑥⑧ B.②④⑥⑦⑨
C.②③⑤⑦⑧ D.①③⑤⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于元素周期表的说法正确的是
A.能生成碱的金属元素都在ⅠA族
B.原子序数为14的元素位于元素周期表的第3周期ⅣA族
C.稀有气体元素原子的最外层电子数均为8
D.第二周期ⅣA族元素的原子核电荷数和中子数一定为6
查看答案和解析>>
科目:高中化学 来源: 题型:
有A、B、C、D四种元素,其原子序数大小关系为A>B>C>D。已知将0.5mol 某元素A原子的最高价离子还原成中性原子时,需得到6.02×1023个电子,当A的单质同盐酸充分反应放出0.02 g氢气时,用去0.4gA单质。A原子中质子数等于中子数。B元素原子的核外电子层数和A相同。C元素的氧化物既溶于强酸,也溶于强碱。D元素的氢化物为DH3。 试回答:
⑴ 元素符号: B C
⑵ C的单质与B的最高价氧化物的水化物溶液反应的化学方程式为
写出A与盐酸反应的离子方程式为
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各项实验操作不能达到目的的是
A.在蔗糖溶液中加入几滴稀硫酸,水浴加热5 min,加入NaOH溶液至碱性,
再加入银氨溶液并水浴加热检验葡萄糖的生成
B.苯中混有苯酚可与足量氢氧化钠溶液反应后分液除去
C.使C2H5Br和NaOH溶液混合后水解,取上层清液,滴加AgNO3溶液检验溴元素
D.只用溴水一种试剂即可鉴别甲苯、己烯、乙醇、四氯化碳四种液体
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应A2(g)+2B2 (g) 2AB2 (g)的ΔH<0,下列说法正确的是( )
2AB2 (g)的ΔH<0,下列说法正确的是( )
A.升高温度,正向反应速率增加,逆向反应速率减小
B.升高温度有利于反应速率增加,从而缩短达到平衡的时间
C.达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动
D.达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质的性质或应用的说法中正确的是 ( )
A.Si是一种非金属主族元素,其氧化物可用于制作计算机芯片
B.胃穿孔患者胃酸过多时,可服用含Al(OH)3的药片
C.Mg、Fe等金属在一定条件下与水反应都生成H2和对应的氢氧化物
D.铝粉和氧化镁粉末混合,高温能发生铝热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
现有五种可溶性物质A、B、C、D、E,它们所含的阴、阳离子互不相同,分别含有五种阳离子Na+、Al3+、Mg2+、Ba2+、Fe3+和五种阴离子Cl-、OH-、NO3-、CO32-、X中的一种。
(1)一同学通过比较分析,认为无需检验就可判断其中必有的两种物质。它们分别是 、 (填化学式)。
(2)为了确定X,现将(1)中的两种物质记为A和B。当C与B的溶液混合时,产生红褐色沉淀和无色无味气体;当C与A的溶液混合时产生二种沉淀,向该沉淀中滴入足量的稀HNO3,沉淀部分溶解,最后留有白色沉淀。
①X为 (填序号)
A.SO32- B.CH3COO- C.SO42- D.SiO32-
②120 mL含有0.20 mol B的溶液和200 mL盐酸,不管将前者滴加入后者,还是将后者滴加入前者,都有气体产生,但最终生成的气体体积不同,则盐酸的浓度合理的是( )
A.2.0mol/L B.1.5 mol/L C.1.8 mol/L D.0.24mol/L
(3)利用上述已经确定的一种物质,可以检验出D、E中的阳离子。请简述实验操作步骤、现象及结论
。
查看答案和解析>>
科目:高中化学 来源: 题型:
实验是研究化学的基础,下图中所示的实验方法、装置或操作完全正确的( )
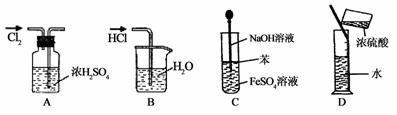
A.干燥Cl2 B.吸收HCl C.制取Fe(OH)2沉淀 D.稀释浓H2SO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com