
(12分)化学兴趣小组用下图所示装置进行探究实验。以验证产物中有乙烯生成且乙烯具有不饱和性。
当温度迅速上后,可观察到试管中的溴水褪色,烧瓶中浓H2SO4与乙醇的混合液体变为棕黑色。(已知:二溴乙烷密度2.18 g·cm-3,不易溶于水,易溶于醇、醚、丙酮等有机溶剂)。
请回答下列问题:
(1)该实验中生成乙烯的化学方程式:_______________________________________。
(2)甲同学认为:该混合液体反应复杂,溴水褪色的现象不能证明反应中有乙烯生成及乙烯具有不饱和性。下列理由中正确的是 __________(填选项)。
A.乙烯与溴水易发生取代反应 B.使溴水褪色的反应,未必是加成反应
C.使溴水褪色的物质,未必是乙烯 D.浓硫酸氧化乙醇生成乙酸,也会使溴水褪色
(3)乙同学对上述实验装置进行了改进,在Ⅰ和Ⅱ之间增加了如下图所示装置。
则A中的试剂应为 ___________ , B中的试剂为____________。
(4)丙同学经过观察后认为:试管中另一现象可证明反应中有乙烯生成,这个现象是:
______________________;为验证这一反应是加成反应而不是取代反应,可用pH试纸来测试反应前后溶液的酸性变化,原理是:_____________________。
(5)处理上述实验后烧瓶中废液,最合理的方法是______________(填选项)。
A.废液经冷却后倒入下水道中 B.废液倒入空废液缸中
C.将水加入烧瓶中稀释后倒入废液缸 D.废液倒入盛有水的塑料桶中,经处理后再倒入下水道
(1)CH3CH2OH  CH2=CH2↑+H2O;(2)B、C;(3)NaOH溶液,品红溶液;(4)试管中液体分层,油状液体在下(或试管中有不溶于水的油状液体产生);若发生取代反应,生成HBr,水溶液pH明显减小;若发生加成反应,水溶液的pH将增大;(5)D
CH2=CH2↑+H2O;(2)B、C;(3)NaOH溶液,品红溶液;(4)试管中液体分层,油状液体在下(或试管中有不溶于水的油状液体产生);若发生取代反应,生成HBr,水溶液pH明显减小;若发生加成反应,水溶液的pH将增大;(5)D
解析试题分析:(1)乙醇与浓硫酸混合加热170℃,发生消去反应制取乙烯。该实验中生成乙烯的化学方程式为CH3CH2OH  CH2=CH2↑+H2O;(2)A.乙烯与溴水易发生加成反应,产生1,2—二溴乙烷,使溴水褪色。能证明反应中有乙烯生成及乙烯具有不饱和性。错误。B.使溴水褪色的反应可能是浓硫酸反应得到SO2反应所致。反应的化学方程式为Br2+2H2O+SO2= SO42-+4H++2Br-。因此不能证明反应中有乙烯生成及乙烯具有不饱和性。正确。C.根据A.B的分析可知使溴水褪色的物质可能是乙烯或SO2.所以不能证明反应中有乙烯生成及乙烯具有不饱和性。正确。D.浓硫酸氧化乙醇生成乙酸,乙酸不会使溴水褪色,因此能证明反应中有乙烯生成及乙烯具有不饱和性。错误。(3)SO2是酸性氧化物,能跟碱发生反应,而乙烯不能反应。所以先通过盛有NaOH溶液的洗气瓶,来除去SO2,然后利用SO2的漂白性,用品红溶液检验SO2已经除去干净。(4)可证明反应中有乙烯生成的现象是试管中液体分层,油状液体在下(或试管中有不溶于水的油状液体产生);若发生取代反应,生成HBr,水溶液pH明显减小;若发生加成反应,水溶液的pH将增大;(5)A.废液中含有大量为反应的硫酸会腐蚀下水道,产生的有机物不处理会污染水源。错误。B.废液倒入空废液缸中,若后来再倒入其它的反应废液,可能会发生反应,产生有害气体而污染大气。错误。C.将水加入烧瓶中,违背浓硫酸的稀释原则,会造成酸滴飞溅,造成危险。错误。D.废液倒入盛有水的塑料桶中,经处理后再倒入下水道,就把危害降低到最小限度。正确。
CH2=CH2↑+H2O;(2)A.乙烯与溴水易发生加成反应,产生1,2—二溴乙烷,使溴水褪色。能证明反应中有乙烯生成及乙烯具有不饱和性。错误。B.使溴水褪色的反应可能是浓硫酸反应得到SO2反应所致。反应的化学方程式为Br2+2H2O+SO2= SO42-+4H++2Br-。因此不能证明反应中有乙烯生成及乙烯具有不饱和性。正确。C.根据A.B的分析可知使溴水褪色的物质可能是乙烯或SO2.所以不能证明反应中有乙烯生成及乙烯具有不饱和性。正确。D.浓硫酸氧化乙醇生成乙酸,乙酸不会使溴水褪色,因此能证明反应中有乙烯生成及乙烯具有不饱和性。错误。(3)SO2是酸性氧化物,能跟碱发生反应,而乙烯不能反应。所以先通过盛有NaOH溶液的洗气瓶,来除去SO2,然后利用SO2的漂白性,用品红溶液检验SO2已经除去干净。(4)可证明反应中有乙烯生成的现象是试管中液体分层,油状液体在下(或试管中有不溶于水的油状液体产生);若发生取代反应,生成HBr,水溶液pH明显减小;若发生加成反应,水溶液的pH将增大;(5)A.废液中含有大量为反应的硫酸会腐蚀下水道,产生的有机物不处理会污染水源。错误。B.废液倒入空废液缸中,若后来再倒入其它的反应废液,可能会发生反应,产生有害气体而污染大气。错误。C.将水加入烧瓶中,违背浓硫酸的稀释原则,会造成酸滴飞溅,造成危险。错误。D.废液倒入盛有水的塑料桶中,经处理后再倒入下水道,就把危害降低到最小限度。正确。
考点:考查乙烯的实验室制法、检验、反应废液的处理等疾病实验操作的知识。


科目:高中化学 来源: 题型:填空题
煤是重要的能源,也是生产化工产品的重要原料。试用所学知识,解答下列问题:
(1)煤的转化技术包括煤的气化技术和液化技术。煤的液化技术又分为 和 。
(2)在煤燃烧前需对煤进行脱硫处理。煤的某种脱硫技术的原理如下图所示:
这种脱硫技术称为微生物脱硫技术。该技术的第一步反应的离子方程式为 ,
第二步反应的离子方程式为 。
(3)工业煤干馏得到的产品有焦炭、 、 等。
(4)湿式石灰石—石膏法脱硫工艺是烟气脱硫技术中最成熟的一种方法。其工艺流程是:烟气经锅炉预热器出来,进入电除尘器除掉大部分粉煤灰烟尘,再经过一个专门的热交换器,然后进入吸收塔,烟气中的SO2与含有石灰石的浆液进行气液接触,通入空气后生成石膏,经脱硫的烟气,应用循环气体加热器进行再加热,进入烟囱,排入大气。
①写出湿法石灰石—石膏法脱硫所涉及的化学反应方程式:__________________________________。
②用石灰石浆液作SO2吸收剂而不用熟石灰吸收SO2的原因是:______________________________。
③上述过程中得到的石膏,如果含氯化合物(主要来源于燃料煤)超过杂质极限值,则石膏产品性能变坏。工业上消除可溶性氯化物的方法是___________________________________________________。
(5)某化学兴趣小组为了测定烟气脱硫所得石膏的组成(CaSO4·xH2O)即测定x值,做如下实验:将石膏加热使之脱水,加热过程中固体的质量与时间的变化关系如图所示。数据表明当固体的质量为2.72g后不再改变。①石膏的化学式为_______________。②图像中AB段对应化合物的化学式为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:问答题
【化学——选修2:化学与技术】(15分)
下列问题涉及煤在化工生产中的应用:
(1)煤的转化技术包括煤的气化技术和液化技术。
煤的液化技术又分为 和
(2)在煤燃烧前需对煤进行脱硫处理。煤的某种脱硫技术的原理如下图所示:
这种脱硫技术称为微生物脱硫技术。该技术的第一步反应的离子方程式为 ;第二步反应的离子方程式为 。
(3)工业煤干馏得到的产品有焦炭、 、 等。
(4)湿式石灰石—石膏法脱硫工艺是烟气脱硫技术中最成熟的一种方法。其工艺流程是:烟气经锅炉预热器出来,进入电除尘器除掉大部分粉煤灰烟尘,再经过一个专门的热交换器,然后进入吸收塔,烟气中的SO2与含有石灰石的浆液进行气液接触,通入空气后生成石膏,经脱硫的烟气,应用循环气体加热器进行再加热,进入烟囱,排入大气。
①写出湿法石灰石—石膏法脱硫所涉及的化学反应方程式:____________________________。
②用石灰石浆液作SO2吸收剂而不用熟石灰吸收SO2的原因是:__________________________
③上述过程中得到的石膏,如果含氯化合物(主要来源于燃料煤)超过 杂质极限值,则石膏产品性能变坏。工业上消除可溶性氯化物的方法是___________________________________。
(5)某化学兴趣小组为了测定烟气脱硫所得石膏的组成(CaSO4·xH2O)即测定x值,做如下实验:将石膏加热使之脱水,加热过程中固体的质量与时间的变化关系如图所示。数据表明当固体的质量为2.72g后不再改变。①石膏的化学式为_______________。②图像中AB段对应化合物的化学式为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
(4分)某烃A的相对分子质量为78,不能使溴水褪色,0.5molA完全燃烧时,得到27g水和67.2L二氧化碳(标准状况)。
求:(1)A的结构简式.(2)写出在催化剂作用下A与H2反应生成C.
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(8分)某化学课外小组用下图装置制取溴苯并探究该反应的类型。先向分液漏斗中加入苯和液溴,再将混合液滴入反应器A(A下端活塞关闭)中。
(1)写出A中反应的化学方程式:________________________________________ 。
(2)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是_________________________。
(3)C中盛放CCl4的作用是_________________________。
(4)若要证明苯和液溴发生的是取代反应,而不
是加成反应,通常有两种方法,请按要求填写下表。
| | 向试管D中加入的试剂 | 能证明苯与液溴发生取代反应的现象 |
| 方法一 | | |
| 方法二 | | |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
实验室制取乙烯,常因温度过高而使乙醇和浓H2SO4反应生成少量的二氧化硫。有人设计下列实验以确认上述混合气体中有乙烯和二氧化硫。其装置如下图所示,试回答下列问题。
(1)图中①、②、③、④装置可盛放的试剂是
①________;②________;③________;④________。(将下列有关试剂的序号填入空格内)
| A.品红溶液 | B.NaOH溶液 |
| C.浓H2SO4 | D.酸性KMnO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关化学反应表达正确的是
A.实验室用液溴和苯在催化剂作用下制溴苯: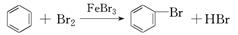 |
| B.蛋壳溶于食醋:CaCO3+CH3COOH===CH3COOCa+H2O+CO2↑ |
C.向CH2BrCOOH中加入足量的氢氧化钠溶液并加热:CH2BrCOOH+OH- CH2BrCOO-+H2O CH2BrCOO-+H2O |
| D.苯酚钠溶液中通入少量CO2:CO2+H2O+2C6H5O-―→2C6H5OH+2CO |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
下面是含有苯环的一系列化合物:
(1)B的化学名称为________,D的分子式为________,上述一系列化合物的分子通式为________。
(2)C的一氯取代物有________种。
(3)上述物质中的某一种可用于制取TNT,该反应的化学方程式为______________________________________________________。
(4)B是制备高分子化合物P的中间产物,下列为工业上制取P的简单流程:
①已知X蒸气的密度是相同条件下甲烷密度的6.5倍,则X的分子式为________。
②上述流程中反应a、b、c的反应类型分别为________、________、________。
③转化X―→P的化学方程式为__________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com