
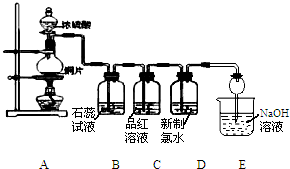
 ij��ѧ��ȤС��Ϊ̽��SO2�Ļ�ѧ���ʣ��������ͼ��ʾ��װ�ý���ʵ�飮�ش��������⣺
ij��ѧ��ȤС��Ϊ̽��SO2�Ļ�ѧ���ʣ��������ͼ��ʾ��װ�ý���ʵ�飮�ش��������⣺���� ��1����Ϥ�������죬˵�������ƣ�ͭ��Ũ�����ڼ��������·�Ӧ��������ͭ��ˮ����������
��2������������������������Һ��Ӧ������ʱӦ��ֹ������
��3����������Ϊ����������ܹ���ˮ��Ӧ���������ᣬ��Һ�����ԣ��ܹ�ʹʯ����ɫ������������л�ԭ�ԣ��ܹ���ԭ��ˮʹ��ˮ��ɫ�����߷�Ӧ������������
��4�������������Ư���ԣ��ܹ�ʹƷ����Һ��ɫ�����������Ư���Ծ��в��ȶ��ԣ��������ָ���ɫ��
��5��ֻͭ����Ũ���ᷴӦ����ϡ�����Ӧ����������������ϡ������ͬһ��Һ��������ͭ���ʣ�
��� �⣺��1��ͼ��A��ʢ��Ũ�������������Ϊ��Һ©���� ͭ��Ũ�����ڼ��������·�Ӧ��������ͭ��ˮ����������ѧ����ʽΪ��Cu+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+SO2��+2H2O��
�ʴ�Ϊ����Һ©���� Cu+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+SO2��+2H2O��
��2������������������������Һ��Ӧ��Eװ���и�����ݻ��ϴ��ܹ���ֹ�����ķ�����
�ʴ�Ϊ����ֹ������
��3����������Ϊ����������ܹ���ˮ��Ӧ���������ᣬ��Һ�����ԣ��ܹ�ʹʯ����ɫ��
����������л�ԭ�ԣ��ܹ���ԭ��ˮʹ��ˮ��ɫ�����߷�Ӧ������������ᣬ���ӷ���ʽ��Cl2+SO2+2H2O=2Cl-+SO42-+4H+��
�ʴ�Ϊ����Һ��ɺ�ɫ�� SO2����ˮ������H2SO3����ԭ��Cl2+SO2+2H2O=2Cl-+SO42-+4H+��
��4�������������Ư���ԣ��ܹ�ʹƷ����Һ��ɫ�����������Ư���Ծ��в��ȶ��ԣ��������ָ���ɫ������
ȡC����Һ������һ�Թ��У����ȣ���Һ�ָֻ���ɫ�����̽��SO2��Ʒ�����õĿ����ԣ�
�ʴ�Ϊ��ȡC����Һ������һ�Թ��У����ȣ���Һ�ָֻ���ɫ��
��5����ַ�Ӧ��С��ͬѧ����ͭ�����ᶼ��ʣ�࣬ԭ�������ŷ�Ӧ���У�Ũ�����ϡ��������ͭ��Ӧ��
��Һ��ʣ��ϡ���ᣬ���������ӣ������������NaNO3���壬���ܹ�����ͭ���������ᡢ����ع��壬������ͭ��Ӧ����ѡ���ڢۣ�
�ʴ�Ϊ�����ŷ�Ӧ���У�Ũ�����ϡ��������ͭ��Ӧ���ڢۣ�
���� ���⿼����ͭ��Ũ����ķ�Ӧ����ϤŨ���ᡢ��������������ǽ���ؼ�����Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ռ���Һ | B�� | ������ | C�� | Ũ���� | D�� | ��̿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Cl2����������NaOH�ǻ�ԭ�� | |
| B�� | ��������Clԭ���뱻��ԭ��Clԭ�ӵĸ�����Ϊ1��5 | |
| C�� | �������뻹ԭ�������ʵ����ı�Ϊ1��2 | |
| D�� | ÿ����1mol��NaClO3ת��6mol�ĵ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ϼʯ��һ�ֹ����Σ�����ɿɱ�ʾΪK2O•3Na2O•4Al2O3•8SiO2��ijС��ͬѧ�����ϼʯΪԭ���Ʊ�Al2O3�ķ������£�
ϼʯ��һ�ֹ����Σ�����ɿɱ�ʾΪK2O•3Na2O•4Al2O3•8SiO2��ijС��ͬѧ�����ϼʯΪԭ���Ʊ�Al2O3�ķ������£��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ʱ�䣨s�� | 0 | 20 | 40 | 60 | 80 |
| n��NO2��/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n��N2O4��/mol | 0.00 | 0.08 | 0.08 |
| A�� | �ӷ�Ӧ��ʼֱ��60s��80sʱ������������ƽ����Ӧ��������ȵ� | |
| B�� | 80s�������������СΪ1L��ƽ��������Ӧ�����ƶ���������ɫ��dz | |
| C�� | n1�ķ�Χ��0.28��n1��0.33 | |
| D�� | �����¶ȣ����ܼӿ췴Ӧ���ʣ�Ҳ�����N2O4��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| V��O2��/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
| A�� | ��Ӧ��6minʱ��c��H2O2��=0.20mol/L | |
| B�� | ��Ӧ��6minʱ��H2O2�ֽ���40% | |
| C�� | 0��6min��ƽ����Ӧ���ʣ�v��H2O2����3.3��10-2mol/��L•min�� | |
| D�� | 6��10min��ƽ����Ӧ���ʣ�v��H2O2����3.3��10-2mol/��L•min�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CH4��C2H4��C3H4 | B�� | C2H4��C3H8��C2H6 | C�� | C2H2��C2H4��C3H6 | D�� | C2H2��C2H6��C3H8 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com