
科目:高中化学 来源: 题型:
| A、100mL2mol/L盐酸与锌反应时,加入100mL氯化钠溶液,生成氢气的速率不变 | B、对于可逆反应2CO+2NO?N2+2CO2,使用合适的催化剂,CO的生成速率和消耗速率都加快 | C、二氧化硫的催化氧化是一个放热反应,升高温度,正反应速率减慢 | D、用铁片和稀硫酸反应制取氢气时,改用铁片和浓硫酸可以加快氢气的产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)若从下列四个地区选址新建一座硫酸厂,最合适的地点应在 附近。?
a.风景旅游区 b.硫酸消耗中心区? c.人口稠密区 d.黄铁矿矿区?
(2)工业生产硫酸的原料气成分(体积分数)为:SO27%,O211%,N2 82%。压强及温度对SO2转化率的影响如下:?
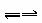
工业上,二氧化硫催化氧化过程采用的是常压而不是高压,主要原因是 。?
分析上表数据可知,二氧化硫的催化氧化是放热反应,理由是 。
(3)据测算,接触法制硫酸过程中,每生产1t 98%的硫酸需消耗3.60×105 kJ能量。若反应:2SO2(g)+O2(g)![]() 2SO3(g),ΔH =-196.6 kJ·mol-1放出的热量完全被利用,则每生产1t 98%的硫酸可为外界提供 kJ能量(不考虑其他过程释放的能量)。?
2SO3(g),ΔH =-196.6 kJ·mol-1放出的热量完全被利用,则每生产1t 98%的硫酸可为外界提供 kJ能量(不考虑其他过程释放的能量)。?
(4)依据题给数据计算:在500 ℃ 0.1 MPa条件下,二氧化硫的催化氧化达到平衡时,各种气体的体积比V(SO2)∶V(SO3)∶V(O2)∶V(N2)= ∶ ∶ ∶ (结果保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
二氧化硫的催化氧化是放热反应。下列关于接触法制硫酸的叙述中正确的是
A .为提高SO2的转化率,接触室内反应温度选定在400℃~500℃
B.为防止催化剂中毒,炉气在进入接触室之前需要净化
C.为防止污染大气,从吸收塔出来的尾气常用NaOH溶液吸收
D.为提高SO3的吸收效率,用稀硫酸代替水吸收SO3 .
查看答案和解析>>
科目:高中化学 来源:2014届广东省高一下学期期末考试化学试卷(解析版) 题型:选择题
下列有关化学反应速率的说法中,正确的是
A. 100 mL 2 mol/L盐酸与锌反应时,加入适量的氯化钠溶液,生成氢气的速率不变
B. 对于可逆反应2CO + 2NO  N2
+ 2CO2,使用合适的催化剂,CO的生成速率和消耗速率都加快
N2
+ 2CO2,使用合适的催化剂,CO的生成速率和消耗速率都加快
C. 二氧化硫的催化氧化是一个放热反应,升高温度,正反应速率减慢
D. 用铁片和稀硫酸反应制取氢气时,改用铁片和浓硫酸可以加快氢气的产生
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com