
 .
.


 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:
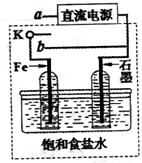 (2013?淄博二模)海水是丰富的资源宝库,从海水中提取元素是化学工业的重要组成部分.
(2013?淄博二模)海水是丰富的资源宝库,从海水中提取元素是化学工业的重要组成部分.查看答案和解析>>
科目:高中化学 来源:2013-2014学年湖南省怀化市高三第一次模拟考试理综化学试卷(解析版) 题型:填空题
海洋是一个丰富的资源宝库,通过海水的综合利用可获得许多物质供人类使用。
(1) 海水中盐的开发利用:
Ⅰ.海水制盐目前以盐田法为主,建盐田必须选在远离江河入海口,多风少雨,潮汐落差大且又平坦空旷的海滩。所建盐田分为贮水池、蒸发池和_______池。
II.目前工业上采用比较先进的离子交换膜电解槽法进行氯碱工业生产,在电解槽中阳离子交换膜只允许阳离子通过,阻止阴离子和气体通过,请说明氯碱生产中阳离子交换膜的作用____________________________________________。(写一点即可)
(2) 电渗析法是近年来发展起来的一种较好的海水淡化技术,其原理如下图所示。请回答后面的问题:
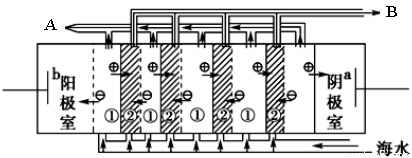
Ⅰ.海水不能直接通入到该装置中,理由是_____________________________________________。
Ⅱ. B口排出的是________(填“淡水”或“浓水”)。
(3) 用苦卤(含Na+、K+、Mg2+、Cl-、Br-等离子)可提取溴,其生产流程如下:
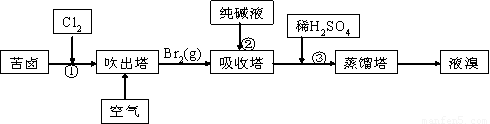
Ⅰ.若吸收塔中的溶液含BrO3-,则吸收塔中反应的离子方程式为_____________
_________________________________________。
Ⅱ.通过①氯化已获得含Br2的溶液,为何还需经过吹出、吸收、酸化来重新获得含Br2的溶液?_____________________________________________________________________。
Ⅲ.向蒸馏塔中通入水蒸气加热,控制温度在900C左右进行蒸馏的原因是___________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年山东省淄博市高三复习阶段性检测(二模)理科综合化学试卷(解析版) 题型:填空题
海水是丰富的资源宝库,从海水中提取元素是化学工业的重要组成部分。
(1)粗盐精制就是除去其中的Ca2+、Fe3+、SO42-及泥沙等杂质,需加入的试剂有:①Na2CO3溶液 ②HCl(盐酸) ③Ba(OH)2溶液,这三种试剂的添加顺序是_________(填序号)。
(2)用氯气进行“海水提溴”中制取溴单质反应的离子方程式为:__________。
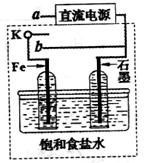
(3)某同学设计了如图装置进行以下电化学实验。
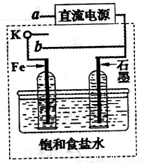
①当开关K与a连接时,两极均有气泡产生,则阴极为_______极。
②一段时间后,使开关K与a断开、与b连接时,虚线框内的装置可称为__________。请写出此时Fe电极上的电极反应式_________________。
(4)某公厂向盛有CaSO4悬浊液的反应池中通入氨气欲制取氮肥(NH4)2SO4,效果不好。再通入CO2,则逐渐产生大量(NH4)2SO4。请分析其原因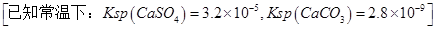 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
海水是丰富的资源宝库,从海水中提取元素是化学工业的重要组成部分。
(1)粗盐精制就是除去其中的Ca2+、Fe3+、SO42-及泥沙等杂质,需加入的试剂有:①Na2CO3溶液 ②HCl(盐酸) ③Ba(OH)2溶液,这三种试剂的添加顺序是_________(填序号)。
(2)用氯气进行“海水提溴”中制取溴单质反应的离子方程式为:__________。
(3)某同学设计了如右图装置进行以下电化学实验。
①当开关K与a连接时,两极均有气泡产生,则阴极为_______极。
②一段时间后,使开关K与a断开、与b连接时,虚线框内的装置可称为__________。请写出此时Fe电极上的电极反应式_________________。
(4)某公厂向盛有CaSO4悬浊液的反应池中通入氨气欲制取氮肥(NH4)2SO4,效果不好。再通入CO2,则逐渐产生大量(NH4)2SO4。请分析其原因![]() 。
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com