
【题目】由CO2、H2O(g)组成的混合气体共a mol,其中CO2的物质的量分数为x.将该混合气体缓慢通过装有1mol Na2O2的真空管,充分反应后,维持120℃、1.01×105Pa.收集所得气体,冷却、称量,真空管中固体质量增加y g.
(1)若a=1,则y=(用含x代数式表示);
(2)若a=2,x=0.5时,反应后所得气体的成份是;
(3)若a=2,y=28时,则x的取值范围;
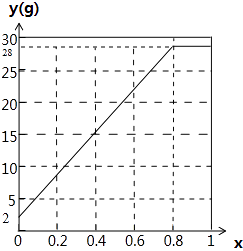
(4)若a=1.25,试作出y与x的关系曲线,并在y轴标明曲线起点和终点的数值.
【答案】
(1)26x+2
(2)氧气、水
(3)0.5≤x<1
(4)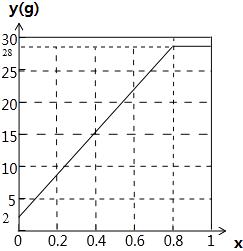
【解析】解:(1)由反应2CO2+2Na2O2=2Na2CO3+O2,2H2O+2Na2O2=4NaOH+O2↑可知,气体与过氧化钠都按1:1反应,a=1时,混合气体与过氧化钠恰好反应,n(CO2)=ax=x,固体增重为y=28n(CO2)+2[1﹣n(CO2)]=28x+2(1﹣x)=26x+2,所以答案是:26x+2;(2)a=2,x=0.5时,n(CO2)=1mol,二氧化碳与过氧化钠恰好反应,水不反应,从Na2O2的真空管出来的气体有氧气、水蒸气,所以答案是:氧气、水;(3)a=2,y=28时,若x≥0.5,水不参加反应,根据过氧化钠计算增重为y=28n(Na2O2)=28,故0.5≤x<1,固体增重28g;若<0.5,二氧化碳完全反应,参加反应的水为[1﹣n(CO2)]mol,所以固体增重为y=28n(CO2)+2[1﹣n(CO2)]=28×2x+2(1﹣2x)=28,解得x=2,不符合题意,所以答案是:0.5≤x<1;(4)当a=1.25时,若x≥0.8,水不参加反应,根据过氧化钠计算增重为y=28n(Na2O2)=28;若x<0.8,二氧化碳完全反应,参加反应的水为[1﹣n(CO2)]mol,所以固体增重为y=28n(CO2)+2[1﹣n(CO2)]=28×2x+2(1﹣2x)=52x+2,当x=0时中含有氢气,y=2,y与x的关系曲线图为:


 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是元素周期表中原子序数依次增大的四种短周期元素,其相关信息如下表:
元素 | 相关信息 |
X | X的单质为密度最小的气体 |
Y | Y的氢化物的水溶液呈碱性 |
Z | Z是地壳中含量最高的元素 |
W | W的一种核素的质量数为35,中子数为18 |
(1)W在元素周期表中的位置_________________。
(2)X与Y可形成一种化合物Y2X4,请写出该化合物的电子式__________,工业合成Y的简单氢化物的化学方程式为________________。
(3)X和Z组成的既含有极性共价键又含有非极性共价键的化合物的结构式是______________;此化合物还可将碱性工业废水中的CN-氧化为碳酸盐和氨,相应的离子方程式为______________
(4)写出铜和Y的最髙价氧化物的水化物的稀溶液反应的离子方程式______________。
(5)W最高价氧化物的水化物的浓溶液不稳定,受热可分解,产物之一是黄绿色气体,且当有28 mol电子发生转移时,共产生9 mol气体,写出该反应的化学方程式______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.A、B、C、D、E为原子序数依次增大的短周期元素,已知A、B、E 3种原子最外层共有11个电子,且这3种元素的最高价氧化物的水化物两两皆能发生反应生成盐和水,C元素的最外层电子数比次外层电子数少4,D元素原子次外层电子数比最外层电子数多3。
(1)A在空气中燃烧生成原子个数比为1:1的化合物,写出其电子式为_______,写出E元素的同族短周期元素的单质与水反应的化学方程式______________。
(2)写出D、E两元素最高价氧化物对应水化物的酸性强弱_________(用化学式表示)。
Ⅱ.在遭遇冰雪灾害时,常使用一种融雪剂,其主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1 mol XY2含有54 mol电子。
(1)该融雪剂XY2的形成过程是________________,X元素在周期表的位置是_______。
(2)元素Q、W原子的最外层电子数是其电子层数的2倍,Q与Y相邻,则Q的离子结构示意图是_______;Q与W能形成一种结构类似于CO2的三原子分子,且每个原子均达到了8e-稳定结构,该分子的电子式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列正确的是( )
A. 氧化还原反应中有一种元素被氧化时,一定有另一种元素被还原
B. 有电子转移的化学反应是氧化还原反应
C. 氧化还原反应中的反应物不是氧化剂,就是还原剂
D. 有单质参加或生成的化学反应一定是氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取NaHCO3和Na2O2的固体混合物x g放入一密闭容器中加热至250℃,充分反应后排出所有气体.将反应后的固体分成完全相同的两份,将其中一份投入到足量的BaCl2溶液中,最后可得到3.94g沉淀.另一份溶于适量的水,无气体放出,再向水溶液中缓慢逐滴加入某物质的量浓度的盐酸,产生气体与所加盐酸体积之间的关系如图所示.试回答下列问题: 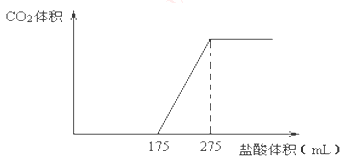
(1)加入盐酸后总共产生的气体在标准状况下的体积为L;
(2)盐酸中HCl的物质的量浓度;
(3)反应后的固体的成分(填化学式);
(4)x= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于如图所示装置的叙述,正确的是( ) 
A.Cu为负极,Zn为正极
B.电子从铜片经外电路流向锌片
C.负极反应为:Zn﹣2e﹣═Zn2+
D.该装置将电能转化为化学能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水(H2O)在很多化学反应中具有极其重要的作用.请研究下列水参与的氧化还原反应.
①NaH+H2O═NaOH+H2↑
②2Na2O2+2H2O═4NaOH+O2↑
③Na+2H2O═2NaOH+H2↑
④3NO2+H2O═2HNO3+NO
⑤2H2O ![]() 2H2↑+O2↑
2H2↑+O2↑
⑥2F2+2H2O═4HF+O2
水只作氧化剂的是;水只作还原剂的是;水既作氧化剂,又作还原剂的是;水既不作氧化剂,又不是还原剂的是
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E五种短周期元素,它们的原子序数依次增大。已知A和B原子具有相同的电子层数,且A元素的最高正价与最低负价和为零,C是同周期中原子半径最大的元素,D是同周期中离子半径最小的元素。C的单质在加热条件下与B的单质充分反应,可以得到与E单质颜色相同的淡黄色固态化合物F。试根据以上叙述回答:
(1)D元素在周期表中位置为_____________________;
(2)画出E的离子结构示意图_____________;写出ABE分子的结构式____________;
(3)工业上常用在微波条件下用A单质与EB2反应来解决其产生的环境问题,写出该化学方程式:___________________________________________;
(4)用电子式表示C2E的形成过程__________________________________________;
(5)1 mol F与A元素的最高价氧化物反应时转移的电子数为_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com