
【题目】在一定体积的密闭容器中放入20L气体P和37L气体W, 在一定条件下发生反应:3P(g)+4W(g) = 4R(g)+nY(g)反应完全后,容器温度不变,混合气体的压强是原来的92.5%,则化学方程式中的n值是
A. 3 B. 2 C. 5 D. 4
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】反应N2O4(g)2NO2(g)△H=+57kJmol﹣1 , 在温度为T时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的为( ) 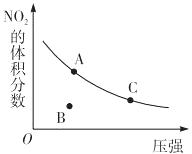
A.A,C两点的反应速率:v(A)>v(C)
B.A,C两点气体的颜色:A深,C浅
C.B点正逆反应速率:v(正)>v(逆)
D.A,C两点气休的平均相对分子质量:A>C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A. Cl2通入水中:Cl+H2O![]() 2H++Cl-+ClO-
2H++Cl-+ClO-
B. 铝粉投入到NaOH溶液中:2Al+2OH-=2AlO2-+H2↑
C. NaHCO3溶液跟足量的Ca(OH)2反应:HCO3-+Ca2++OH-=CaCO3↓+H2O
D. H2SO4溶液中加入足量的Ba(OH)2溶液:SO42-+H++Ba2++OH-=BaSO4↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是向MgCl2和AlCl3的混合溶液中加入NaOH溶液和盐酸时沉淀的物质的量y mol与加入NaOH溶液和盐酸的体积x mL的关系图,根据图示判断,下列结论中不正确的是

A. N点时溶液中的溶质只有NaCl
B. 原混合溶液中c (MgCl2)∶c (AlCl3)=1∶2
C. c (NaOH)=c (HCl)
D. M点之前加入的是NaOH溶液,M点之后加入的是盐酸
【答案】B
【解析】由图象可知N→M发生Al(OH)3+OH-===AlO2-+2H2O,设氢氧化钠溶液浓度为c,则消耗氢氧化钠0.01cmol,n[Al(OH)3]=n(AlCl3)=0.01cmol;ON消耗氢氧化钠0.05cmol,分别发生MgCl2+2NaOH=Mg(OH)2↓+2NaCl、AlCl3+3NaOH=Al(OH)3↓+3NaCl,可知n(MgCl2)=(0.05cmol-0.01c×3mol)/2=0.01cmol,则c(AlCl3):c(MgCl2)=1:1,M点时溶液成分为NaAlO2,之后继续加入溶液后沉淀质量逐渐增大,此时应加入盐酸,发生反应为:NaAlO2+HCl+H2O= Al(OH)3↓+NaCl,继续加入盐酸沉淀逐渐溶解,生成氯化镁、氯化铝和氯化钠,则消耗的氢氧化钠和HCl的物质的量相等,A.根据分析可知,N点时溶液中的溶质只有NaCl,A正确;B.原混合溶液中c(MgCl2):c(AlCl3)=1:1,B错误;C.由横坐标可知消耗盐酸和氢氧化钠的体积相同,则二者物质的量浓度相同,C正确;D.根据分析可知,M点之前加入的是NaOH溶液,M点之后加入的是盐酸,D正确;答案选B。
【题型】单选题
【结束】
16
【题目】证明某溶液中只含有Fe2+而不含有Fe3+的实验方法是
①先滴加氯水,再滴加KSCN溶液后显红色
②先滴加KSCN溶液,不显红色,再滴加氯水后显红色
③滴加NaOH溶液,先产生白色沉淀,后变灰绿,最后呈红褐色
④只需滴加KSCN溶液
A. ①② B. ②③ C. ③④ D. ①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧元素有三种核素16O、17O、18O,它们在自然界中所占的原子个数百分比分别为a%、b%、c%,则下列说法正确的是( )
A.一个16O原子的质量为16g
B.17O的相对原子质量约为17
C.氧元素的相对原子质量为 ![]()
D.氧元素的相对原子质量为(16a%+17b%+18c%)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《本草衍义》中对精制砒霜过程有如下叙述,“取砒之法,将生砒就置火上,以器覆之,令砒烟上飞着覆器,遂凝结累然下垂如乳,尖长者为胜,平短者次之。”文中涉及的操作方法是
A. 蒸馏 B. 升华 C. 过滤 D. 萃取
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组对一含有Al3+的未知溶液进行了如下分析:①滴入少量氢氧化钠溶液,无明显变化;②继续滴加氢氧化钠溶液,开始产生白色沉淀;③滴入过量的氢氧化钠溶液,白色沉淀明显减少。实验小组经定量分析,绘出沉淀的物质的量与滴入氢氧化钠体积的关系图。则下列说法中错误的是( )

A. 该未知溶液中至少含有3种阳离子
B. 滴加的NaOH溶液的物质的量浓度为5 mol/L
C. 若另一种离子为二价阳离子,则a=5
D. 最终得到的沉淀,其成分无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有两个实验小组的同学为探究过氧化钠与二氧化硫的反应,都用如下图所示的装置进行实验.通入SO2气体,将带余烬的木条插入试管C中,木条复燃.请回答下列问题:
(1)第1小组同学认为Na2O2与SO2反应生成了Na2SO3和O2 , 该反应的化学方程式是 .
(2)请设计一种实验方案证明Na2O2与SO2反应生成的白色固体中含有Na2SO3 . .
(3)第2小组同学认为Na2O2与SO2反应除了生成Na2SO3和O2外,还有Na2SO4生成.为检验是否有Na2SO4生成,他们设计了如下方案:将B中反应后的固体溶解于水 ![]() 白色沉淀
白色沉淀 ![]() 仍有部分白色沉淀不溶解,证明有Na2SO4生成
仍有部分白色沉淀不溶解,证明有Na2SO4生成
上述方案是否合理? . 请简要说明两点理由:
①;② .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为了探究常温下某非金属氧化物形成的未知气体的成分.该小组成员将气体通入澄清石灰水,发现澄清石灰水变浑浊,持续通入发现浑浊又变澄清,由此该小组成员对气体的成分提出猜想.
(1)【提出猜想】
猜想1:
猜想2:
猜想3:
为了验证猜想,该小组设计实验加以探究.
【实验探究】该小组同学按如图所示装置,将气体从a端通入,则;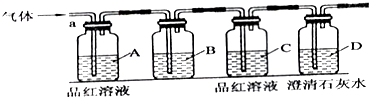
(2)B中应该装试剂(填编号).
A.氢氧化钠溶液
B.酸性高锰酸钾溶液
C.饱和碳酸钠溶液
D.饱和碳酸氢钠
(3)A中品红溶液的作用是 .
(4)D中澄清石灰水的作用是 .
(5)通过该实验,该小组同学观察到以下三个实验现象:
①A中品红溶液褪色 ②C中品红溶液不褪色 ③D中澄清石灰水变浑浊
【得出结论】由上述现象该小组同学确认该气体为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com