
分析 (1)小苏打与烧碱溶液反应生成碳酸钠和水;
(2)钠和水反应生成氢氧化钠和氢气;
(3)过量的二氧化碳通入氢氧化钠溶液中,反应生成碳酸氢钠;
(4)Na2CO3溶液与CH3COOH溶液反应,反应生成醋酸钠和二氧化碳、水;
(5)大理石(CaCO3)与稀HNO3反应生成硝酸钙、二氧化碳和水;
(6)Al与NaOH溶液反应生成偏铝酸钠和氢气;
(7)AgNO3溶液与NaCl溶液反应生成硝酸钠和氯化银沉淀;
解答 解:(1)小苏打与烧碱溶液反应生成碳酸钠和水,离子方程式:HCO3-+OH-=CO32-+H2O;
故答案为:HCO3-+OH-=CO32-+H2O;
(2)钠和水反应生成氢氧化钠和氢气,离子方程式:2Na+2H2O=2Na++2OH-+H2↑;
故答案为:2Na+2H2O=2Na++2OH-+H2↑;
(3)过量的二氧化碳通入氢氧化钠溶液中,反应生成碳酸氢钠,离子方程式:CO2+OH-=HCO3-;
故答案为:CO2+OH-=HCO3-;
(4)Na2CO3溶液与CH3COOH溶液反应,反应生成醋酸钠和二氧化碳、水,离子方程式CO32-+2CH3COOH=CO2↑+2CH3COO-+H2O;
故答案为:CO32-+2CH3COOH=CO2↑+2CH3COO-+H2O;
(5)大理石(CaCO3)与稀HNO3反应生成硝酸钙、二氧化碳和水,离子方程式:CaCO3+2H+=Ca2++CO2↑+H2O;
故答案为:CaCO3+2H+=Ca2++CO2↑+H2O;
(6)Al与NaOH溶液反应生成偏铝酸钠和氢气,离子方程式:2Al+2OH-+2H2O=2AlO2-+3H2↑;
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(7)AgNO3溶液与NaCl溶液反应生成硝酸钠和氯化银沉淀,离子方程式:Ag++Cl-=AgCl↓;
故答案为:Ag++Cl-=AgCl↓.
点评 本题考查了离子方程式的书写,明确物质的性质及发生的反应,熟悉离子方程式书写注意问题是解题关键,注意化学式拆分,题目难度不大.


 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | N2O | B. | N2 | C. | NO | D. | NO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若有0.2mol氧化剂反应,则转移电子的物质的量为1.0mol | |
| B. | 若氧化产物比还原产物多0.35mol,生成8.96LN2(标准状况) | |
| C. | 若氧化产物比还原产物多0.35mol,有0.050molKNO3被氧化 | |
| D. | KNO3的氧化性强于N2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1:1 | B. | 1:1:3 | C. | 1:3:1 | D. | 3:1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 摩尔是国际单位制中的一种物理量 | B. | 摩尔是物质的量的单位 | ||
| C. | 摩尔简称摩,它的符号是mol | D. | 1 mol氧原子可表示为“1 mol O” |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 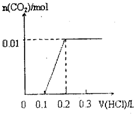 | B. | 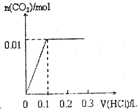 | C. | 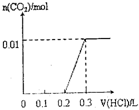 | D. | 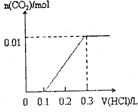 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100mL 8mol/LFeCl3溶液完全反应可制得0.8NA 个Fe(OH)3胶粒 | |
| B. | 0.1 mol 16OD-离子含有的电子、中子数均为1.0NA | |
| C. | 常温常压下,42g乙烯和丁烯混合气体中,极性键数为 6 NA | |
| D. | 密闭容器中2 mol NO与1 mol O2充分反应,产物的分子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在反应3Br2+3CO32-=5Br-+BrO3-+3CO2↑中,每生成3 mol CO2转移的电子数为5NA | |
| B. | 0.5 mol 甲基中电子数为5NA | |
| C. | 常温下,1 L 0.1 mol/L的NH4NO3溶液中氢原子总数为0.4NA | |
| D. | 常温常压下,22.4 L N2H4中N-H键数为4NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com