
| A、均存在电离平衡与水解平衡 |
| B、c(OH-):①>② |
| C、存在的粒子种类相同 |
| D、②溶液中:c(HCO3-)>c(H2CO3) |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、生成了一种强酸弱碱盐 |
| B、等浓度的强酸和弱碱溶液反应 |
| C、浓的弱酸溶液和稀的强碱溶液反应 |
| D、浓的强酸和稀的强碱溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将电源反接前a极发生的反应为:2H++2e-=H2↑ |
| B、将电源反接后,a极发生的反应只有Cu2++2 e-=Cu |
| C、整个电解过程只产生一种气体 |
| D、原硫酸铜溶液的浓度为2.5mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验编号 | T/℃ | n(CO)/n(H2) | p/MPa |
| ⅰ | 150 | 1/3 | 0.1 |
| ⅱ | 5 | ||
| ⅲ | 350 | 5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、4.6g钠投入45.4g水中 |
| B、6.2g氧化钠投入42.2g水中 |
| C、7.8g过氧化钠投入42.2g水中 |
| D、8g烧碱投入42g水中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
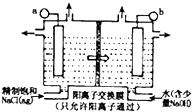 ClO2为一种黄绿色气体,是目前国际上公认的高效,广谱,快速安全的杀菌剂.制备ClO2的新工艺是电解法.
ClO2为一种黄绿色气体,是目前国际上公认的高效,广谱,快速安全的杀菌剂.制备ClO2的新工艺是电解法.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com