
 (3)你认为B、C、D元素形成的化合物之间_________(填“能”或“不能”)发生下面的反应BC+BD3 D BC2+D2C,得出上面结论的理由是________________。
(3)你认为B、C、D元素形成的化合物之间_________(填“能”或“不能”)发生下面的反应BC+BD3 D BC2+D2C,得出上面结论的理由是________________。 (4)Ⅰ.恒温恒压下,在一体积可变的密闭容器中发生下列反应:
(4)Ⅰ.恒温恒压下,在一体积可变的密闭容器中发生下列反应: 4NO+5H2O
4NO+5H2O 4NO+5H2O
4NO+5H2O

科目:高中化学 来源:不详 题型:单选题
 2AB;在温度和压强可变条件下,产物AB的生成情况如图所示:a为500 ℃,b为300 ℃,从t3开始压缩容器,则下列叙述正确的是
2AB;在温度和压强可变条件下,产物AB的生成情况如图所示:a为500 ℃,b为300 ℃,从t3开始压缩容器,则下列叙述正确的是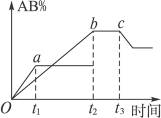
| A.AB为气体,A2、B2中必有一种为非气体;正反应吸热 |
| B.AB为气体,A2、B2中必有一种为非气体;正反应放热 |
| C.AB为固体,A2、B2中必有一种为非气体;正反应放热 |
| D.A2、B2、AB均为气体;正反应吸热 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
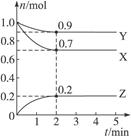
| A.X+Y====2Z;0.05 mol·L-1·min-1 |
| B.X+Y====2Z;0.1 mol·L-1·min-1 |
| C.X+2Y====Z;0.1 mol·L-1·min-1 |
| D.X+3Y====2Z;0.05 mol·L-1·min-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 pC(g)在不同温度(T)、压强(P)下,生成物C的物质的量分数x(C)的变化情况。下列关于该正反应热效应及方程式中A、B、C的化学计量数的判断中,正确的是
pC(g)在不同温度(T)、压强(P)下,生成物C的物质的量分数x(C)的变化情况。下列关于该正反应热效应及方程式中A、B、C的化学计量数的判断中,正确的是 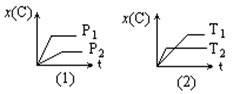
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
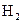 的总量,可采取的措施是( )
的总量,可采取的措施是( )A.加入少量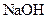 固体 固体 | B.加入少量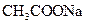 固体 固体 |
C.加入少量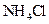 固体 固体 | D.加入少量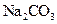 固体 固体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 H2(g)+I2(g)已达到平衡状态的是( )
H2(g)+I2(g)已达到平衡状态的是( )查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Cl2溶于水的反应 |
| B.氢气和氧气的反应 |
| C.电解水生成H2和O2,点燃H2和O2的混合物生成H2O |
| D.实验室加热二氧化锰和浓盐酸的混合物制取氯气的反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com