
| 0min | 10min | 20min | 30min | 40min | 50min | |
| 830℃ | 1mol | 0.8mol | 0.65mol | 0.55mol | 0.5mol | 0.5mol |
| 1100℃ | 1mol | 0.75mol | 0.6mol | 0.6mol | 0.6mol | 0.6mol |
| ||
| △t |
| ||
| 40min |
| 反应的CO的物质的量 |
| 反应初始时CO的总的物质的量 |
| (1-0.5)mol |
| 1mol |
| 0.6mol |
| 1L |
| C(CO).C(H2O) |
| C(H2).C(CO2) |
| 0.6mol/L×0.6mol/L |
| 0.4mol/L×0.4mol/L |
| 9 |
| 4 |
| 9 |
| 4 |
| 1mol |
| 2L |
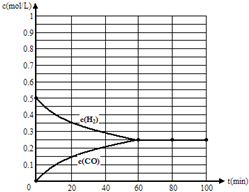 ,
, .
.

科目:高中化学 来源:不详 题型:单选题
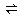 2NH3,用υ(H2)和υ(N2)分别表示其中的化合反应的速率,用υ(NH3)表示其中分解反应的速率。下列能说明反应已达到平衡状态的是( )
2NH3,用υ(H2)和υ(N2)分别表示其中的化合反应的速率,用υ(NH3)表示其中分解反应的速率。下列能说明反应已达到平衡状态的是( )| A.3υ(N2)=υ(H2) | B.υ(H2)=υ(NH3) |
| C.2υ(H2)=3υ(NH3) | D.υ(N2)=3υ(H2) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
 CO2+H2,达到平衡时,
CO2+H2,达到平衡时,查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
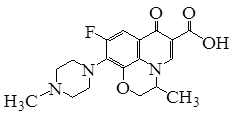
| A.能发生加成、取代反应 |
| B.能发生还原、酯化反应 |
| C.分子内共有19个氢原子 |
| D.分子内共平面的碳原子多于6个 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com