
分别用X、Y、Z、W四种金属进行如下三个实验:
|


科目:高中化学 来源: 题型:
 2Z(g)达到平衡时,各物质的平衡浓度为c(X)=0.5mol/L;c(Y)=0.1mol/L; c (Z)=1.6mol/L若用a、b、c 分别表示X Y Z的初始浓度(mol/L)则a、b应满足的关系是
2Z(g)达到平衡时,各物质的平衡浓度为c(X)=0.5mol/L;c(Y)=0.1mol/L; c (Z)=1.6mol/L若用a、b、c 分别表示X Y Z的初始浓度(mol/L)则a、b应满足的关系是 dD(g)+eE(g),建立平衡后,维持温度不变而压强改变,测得D的浓度变化如下:
dD(g)+eE(g),建立平衡后,维持温度不变而压强改变,测得D的浓度变化如下:| 压强(Pa) | 4×105 | 6×105 | 10×105 | 20×105 |
| D的浓度(mol/L) | 0.085 | 0.126 | 0.200 | 0.440 |
查看答案和解析>>
科目:高中化学 来源: 题型:
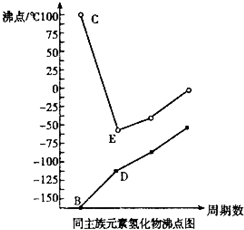 X、Y、Z、W是原子序数依次增大的四种短周期元素,X和Z,Y和W分别同主族.B、C、D、E分别为X、Y、Z、W的氢化物,它们的沸点如图
X、Y、Z、W是原子序数依次增大的四种短周期元素,X和Z,Y和W分别同主族.B、C、D、E分别为X、Y、Z、W的氢化物,它们的沸点如图查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 | 将X与Y用导线连接,浸入电解质溶液中,Y不易腐蚀 |
| 2 | 将X、W分别投入等浓度的稀盐酸中都有气体产生,但W比X反应剧烈 |
| 3 | 用惰性电极电解含等物质的量浓度的Y2+和Z2+混合溶液,在阴极上首先析出单质Z |
| A、Z2+的氧化性可能最强 |
| B、W的金属活动性强于Y |
| C、Z放入CuSO4溶液中一定有Cu析出 |
| D、用X、Z和稀硫酸构成的原电池,X做负极 |
查看答案和解析>>
科目:高中化学 来源:2010-2011学年河北省衡水中学高一下学期期末考试化学试卷 题型:填空题
(13分)
Ⅰ 某温度下,密闭容器中充入1 mol N2和3 mol H2,使之反应合成NH3,平衡后,测得NH3的体积分数为w,如果温度不变,只改变起始加入量,使之反应平衡后NH3的体积分数仍为w,N2、H2、NH3的物质的量分别用x、y、z表示.
(1)恒温恒容条件下:若x=0.75 mol, 则y=________,z=________.
(2)恒温恒压条件下,x、y、z(均不小于0)满足的一般条件是_______________________.
Ⅱ 一定条件下,可逆反应X(g)+Y(g) 2Z(g)达到平衡时,各物质的平衡浓度为c(X)=0.5mol/L;c(Y) ="0.1" mol /L ; c (Z)="1.6" mol /L若用a、b、c 分别表示X Y Z的初始浓度(mol/L)则a、b应满足的关系是________ ____, a的取值范围为_______________
2Z(g)达到平衡时,各物质的平衡浓度为c(X)=0.5mol/L;c(Y) ="0.1" mol /L ; c (Z)="1.6" mol /L若用a、b、c 分别表示X Y Z的初始浓度(mol/L)则a、b应满足的关系是________ ____, a的取值范围为_______________
Ⅲ 在10℃和4×105Pa的条件下,当反应aA(g) dD(g)+eE(g),建立平衡后,维持温度不变而压强改变,测得D的浓度变化如下:
dD(g)+eE(g),建立平衡后,维持温度不变而压强改变,测得D的浓度变化如下:
| 压强(Pa) | 4×105 | 6×105 | 10×105 | 20×105 |
| D的浓度(mol/L) | 0.085 | 0.126 | 0.200 | 0.440 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com