
二氧化氯(ClO2)是一种高效消毒剂,沸点为11℃。用氯酸钾粉末与草酸在60℃时反应可生成二氧化氯等物质,实验装置如下图所示:

(1)装置A中还应安装的玻璃仪器是 ,装置B用冰水浴的原因是 。
(2)装置A中产物有K2CO3、ClO2和CO2等,请写出该反应的化学方程式: 。
(3)①实验过程中,装置C中少量的ClO2与NaOH溶液反应产生两种钠盐,且物质的量之比为1:1,其中一种为NaClO2,写出装置C中生成这两种钠盐的离子方程式: 。
②饱和溶液在温度低于38℃时析出晶体NaClO2?3H2O,在温度高于38℃时析出晶体NaClO2。请补充从NaClO2溶液中制得NaClO2晶体的操作步 骤:
骤:
a. ;b. ;c.洗涤;d.干燥。
(4)还可采用盐酸或双氧水还原氯酸钠制备ClO2。用H2O2作还原剂制备ClO2更受欢迎,其主要原因是 。
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:高中化学 来源:2016届黑龙江省高三第一阶段考试理综化学试卷(解析版) 题型:选择题
铁、铜混合粉末18.0g加入到100ml 5.0mol/LFeCl3溶液中,剩余固体质量为3.2g。下列说法正确的是
A.剩余固体是铁、铜混合物
B.反应后溶液中n(Fe2+)+ n(Cu2+)=0.75 mol
C.反应后溶液中n(Fe3+)=0.10 mol
D.原固体混合物中铜的质量是8.0g
查看答案和解析>>
科目:高中化学 来源:2016届安徽省合肥市高三上第二次段考化学试卷(解析版) 题型:选择题
山萘酚(Kaempf erol)结构如下图所示,且大量存在于水果、蔬菜、豆类、茶叶中,具有多种生物学作用,如抗氧化、抑制肿瘤生长及保护肝细胞等作用。下列有关山萘酚的叙述正确的是
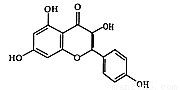
A.结构式中含有羟基、醚键、酯基、碳碳双键
B.可发生取代反应、水解反应、加成反应
C.可与NaOH反应,不能与NaHCO3反应
D.1 mol山萘酚与溴水反应最多可消耗4 mol Br2
查看答案和解析>>
科目:高中化学 来源:2016届河南省高三第四次大考化学试卷(解析版) 题型:实验题
(14分)我国制碱工业的先驱 侯德榜先生,1939年发明了著名的侯氏制碱法,其核心反应原理可用如下化学方程式表示:NH3+CO2+NaCl+H2O=NH4Cl+NaHCO3↓(晶体)依据此原理,欲制得碳酸氢钠晶体,某校学生设计了如下实验装置,其中B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和。
侯德榜先生,1939年发明了著名的侯氏制碱法,其核心反应原理可用如下化学方程式表示:NH3+CO2+NaCl+H2O=NH4Cl+NaHCO3↓(晶体)依据此原理,欲制得碳酸氢钠晶体,某校学生设计了如下实验装置,其中B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和。
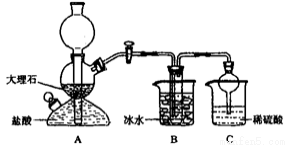
(1)A装置中所发生反应的离子方程式为________。C装置中稀硫酸的作用为_________。
(2)该校学生在检查完此套装置气密性后进行实验,结果没有得到碳酸氢钠晶体,指导教师指出应在装置 之间(填写字母)连接一个盛有 的洗气装置,其作用是 。
(3)过滤NaHCO3 时除烧杯、漏斗外,还用到另一玻璃仪器,该仪器在此操作中的主要作用是 。
(4)若该校学生进行实验时,所用饱和食盐水中含NaCl的质量为5.85g,实验后得到干燥的晶体的质量为5 .04g,则NaHCO3的产率为 。
.04g,则NaHCO3的产率为 。
查看答案和解析>>
科目:高中化学 来源:2016届河南省高三第四次大考化学试卷(解析版) 题型:选择题
下列实验中,依据实验操作及现象,得出的结论正确的是
操 作 | 现 象 | 结 论 | |
A | 测定等浓度的Na2CO3和Na2SO4 溶液的pH | 前者pH比后者的大 | 非金属性: |
B | 将一片铝箔置于酒精灯外焰上灼烧 | 铝箔熔化但不滴落 | 铝箔表面有致密Al2O3薄膜,且Al2O3熔点低于Al |
C | 向溶液X中加入稀盐酸,并将产生的无色气体通入澄清石灰水中 | 生成白色沉淀 | 溶液X中一定含有 |
D | 取久置的Na2O2粉末,向其中滴加过量的盐酸 | 产生无色气体 | Na2O2没有变质 |
查看答案和解析>>
科目:高中化学 来源:2016届河南省洛阳市高三上学期周练化学试卷(解析版) 题型:选择题
(双选)在复盐NH4Fe(SO4)2溶液中逐滴加入Ba(OH)2溶液,可能发生的反应的离子方程式是
A.Fe2++SO42-+Ba2++2OH-=BaSO4↓+Fe(OH)2↓
B.NH4++Fe3++2SO42-+2Ba2++4OH-=2BaSO4↓+ Fe(OH)3↓+NH3•H2O
C.2Fe3++3SO42-+3Ba2++6OH-=3BaSO4↓+2Fe(OH)3↓
D.3NH4++Fe3++3SO42-+3Ba2++6OH-=3BaSO4↓+ Fe(OH)3↓+3NH3•H2O
查看答案和解析>>
科目:高中化学 来源:2016届河北省衡水市高三复习班上月考化学试卷(解析版) 题型:选择题
一般情况下,前者无法决定后者的是
A.原子核外电子排布——元素在周期表中的位置
B.弱电解质的相对强弱——电离常数的大小
C.分子间作用力的大小——分子稳定性的高低
D.物质内部储存的能量高低——化学反应的热效应
查看答案和解析>>
科目:高中化学 来源:2016届甘肃省高三9月月考化学试卷(解析版) 题型:选择题
标准状况下VL氨气溶解在1L水中,所得溶液的密度为ρ g/ml,质量分数为ω,物质浓度为c mol/L,则下列关系中不正确的是
A.ρ =  B.ω =
B.ω = 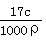
C.ω = 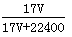 D.c =
D.c = 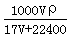
查看答案和解析>>
科目:高中化学 来源:2016届河南省高三上学期开学考试化学试卷(解析版) 题型:填空题
(12分)运用相关原理,回答下列各小题:
(1)25℃时,某FeCl3溶液的pH=2,则此溶液中由水电离产生的c(OH-)= ;用离子方程式表示FeCl3溶液用于净水的原因: 。
(2)已知Ksp(AgCl)=1.8×10﹣10,若向50mL0.018mol•L﹣1的AgNO3溶液中加50mL 0.020mol•L﹣1的盐酸,混合后溶液中Ag+的浓度为 。
(3)NH4HSO4在分析试剂、医药、电子工业中用途广泛。现向100 mL 0.1 mol·L-1NH4HSO4 溶液中滴加0.1 mol·L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图所示。试分析图中a、b、c、d、e五个点,
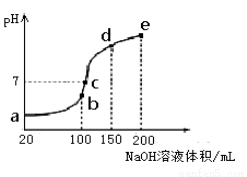
①水的电离程度最大的是_________;
②其溶液中c(OH-)的数值最接近NH3·H2O的电离常数K数值的是 ;
③在c点,溶液中各离子浓度由大到小的排列顺序是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com