
| A、RCl |
| B、RCl2 |
| C、RCl3 |
| D、RCl4 |


 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案 培优三好生系列答案
培优三好生系列答案科目:高中化学 来源: 题型:
| A、分子中的3个碳原子在一条直线上 |
| B、在光照条件下能和氯气发生取代反应 |
| C、充分燃烧的产物是水和二氧化碳 |
| D、丙烷和丁烷互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、回收电池外壳的金属材料 |
| B、回收其中石墨电极 |
| C、不使电池中渗泄的电解液腐蚀其它物品 |
| D、防止电池中汞、镉等重金属离子对土壤和水源的污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+ Al3+ Cl- CO32- |
| B、Ag+ H+ Cl- NO3- |
| C、Fe3+ Na+S2- NO3- |
| D、Cu2+ NH4+ Br- OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Mg>Al>Fe |
| B、Al>Fe>Mg |
| C、Al>Mg>Fe |
| D、Fe>Mg>Al |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠是银白色金属,硬度小,熔点较低 |
| B、金属钠在空气中燃烧,生成过氧化钠 |
| C、NaHCO3比Na2CO3更稳定 |
| D、NaHCO3溶液和Na2CO3溶液可用CaCl2溶液鉴别 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
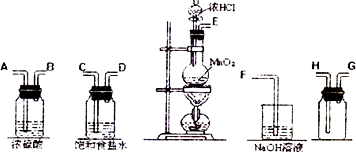
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com