
 如图是M、N两种物质的溶解度曲线.t2℃时往盛有100g水的烧杯中先后加入ag M和ag N(两种物质溶解时互不影响,且溶质仍是M、N),充分搅拌.降温至t1℃,下列说法正确的是( )
如图是M、N两种物质的溶解度曲线.t2℃时往盛有100g水的烧杯中先后加入ag M和ag N(两种物质溶解时互不影响,且溶质仍是M、N),充分搅拌.降温至t1℃,下列说法正确的是( )| A. | t2℃时,得到M的饱和溶液 | |
| B. | t2℃时,得到N的不饱和溶液 | |
| C. | 温度降低到t1℃时,得到M、N的不饱和溶液,且溶液中溶质的质量分数相等 | |
| D. | 温度降低到t1℃时,M、N的溶解度相等,得到M、N的饱和溶液 |
分析 由图象可知,温度大于t1℃时,M的溶解度较大,随着温度的升高,M的溶解度逐渐增大,N的溶解度逐渐减小,温度小于t1℃时,N的溶解度较大,以此解答该题.
解答 解:A.t2℃时,M的溶解度大于ag,M为不饱和溶液,故A错误;
B.t2℃时,N的溶解度为ag,得到饱和溶液,故B错误;
C.温度降低到t1℃时,M、N的溶解度都大于ag,则为不饱和溶液,由于溶质的质量相等,溶液的质量相等,则质量分数相等,故C正确;
D.温度降低到t1℃时,M、N的溶解度都大于ag,都是不饱和溶液,故D错误.
故选C.
点评 本题考查溶解度曲线的意义及饱和溶液、不饱和溶液的判断、溶质质量分数的求法,题目难度不大,注意熟练掌握饱和溶液、不饱和溶液的概念,掌握溶质的质量分数、物质的量浓度的计算方法.


 优学名师名题系列答案
优学名师名题系列答案科目:高中化学 来源: 题型:填空题
 (1)指出使用如表仪器 (已洗净)或用品的第一步操作:
(1)指出使用如表仪器 (已洗净)或用品的第一步操作:| 淀粉-KI试纸检验气体 | 集气瓶收集氨气 | 容量瓶 |
| 用蒸馏水湿润 | 干燥集气瓶 | 检验是否漏水(检漏) |
| 应称量NaOH的质量/g | 应选用容量瓶的规格/mL | 除容量瓶外还需要的其它仪器 |
| 4.0 | 500 | 烧杯、量筒、玻璃棒、药匙、托盘天平、胶头滴管 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等质量的铝分别与足量的盐酸和足量的氢氧化钠溶液反应制得等质量的氢气 | |
| B. | 向氯化铝溶液中滴加过量氨水,最终得到澄清溶液 | |
| C. | 常温下铝、铁都可以与浓硝酸反应制得大量的NO2 | |
| D. | FeCl3溶液加热蒸干得到无水氯化铁晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
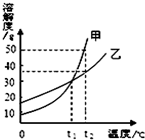
| A. | 甲的溶解度大于乙的溶解度 | |
| B. | 升高温度可使甲的不饱和溶液变为饱和溶液 | |
| C. | t1℃时,甲、乙两种饱和溶液的溶质质量分数相等 | |
| D. | t2℃时,50g乙加入100g水中得到乙的不饱和溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液中K+、Fe2+、SCN-、Br-可以大量存在 | |
| B. | 和KI溶液反应的离子方程式:Fe3++2I-═Fe2++I2 | |
| C. | 和Ba(OH)2溶液反应离子方程式:Fe3++SO42-+Ba2++3OH-═Fe(OH)3↓+BaSO4↓ | |
| D. | 1L0.1 mol•L-1该溶液和足量的Zn充分反应,生成11.2gFe |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com