
【题目】化学用语是表示物质组成、结构和变化规律的一种具有国际性、科学性和规范性的书面语言,化学用语具有简便、确切地表达化学知识和化学思维的特点.下列化学用语中书写正确的是
A. 氯离子的结构示意图:![]()
B. 次氯酸的结构式:H-O-Cl
C. CO2分子的比例模型:![]()
D. 用电子式表示氯化氢分子的形成过程:![]()
科目:高中化学 来源: 题型:
【题目】根据要求填空:
(1)①常温下,.某溶液中由水电离出的c(OH﹣)=1.0×10﹣10mol/L,该溶液可以是 . (填选项)
A.pH=4的CH3COOH
B.pH=10的NaOH
C.pH=9的 Na2CO3
D.pH=2的 H2SO4
E.pH=4的 NH4Cl
(2)在100℃时,将 100mL 0.1mol/L 的稀H2SO4溶液与 100mL 0.4mol/L的NaOH 溶液混合后,溶液的pH= . (混合时溶液体积变化忽略不计,己知Kw=10﹣12).
(3)常温下,amL0.1mol/L盐酸与bmL0.1mol/L氨水混合,充分反应,若混合后溶液呈中性,则ab (填“<”、“>”或“=”).
(4)常温下,amLpH=3的盐酸与bmLpH=11的氨水混合,充分反应,若a=b,则反应后溶液中离子浓度从大到小的顺序是 .
(5)氯化铝水溶液呈酸性,原因是(用离子方程式表示>: . 把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是 .
(6)25℃,在0.10mol/LH2S溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2﹣)关系如下图(忽略溶液体积的变化、H2S的挥发). ①pH=13时,溶液中的 c(H2S)+c(HS﹣)=mol/L.
②某溶液含 0.020mol/LMn2+、0.10mol/LH2S,当溶液pH=时,Mn2+开始沉淀.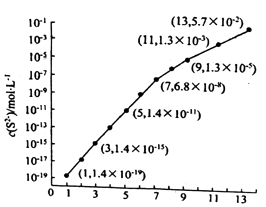
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组要完成中和热的测定.
(1)实验桌上备有大小两个烧杯、泡沫塑料、泡沫塑料板、胶头滴管、量筒、0.5molL﹣1盐酸、0.55molL﹣1NaOH溶液,实验尚缺少的玻璃用品是 .
(2)①实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒?(填“能”或“否”),其原因是 . ②在大、小烧杯之间填满碎泡沫塑料的作用是 .
(3)他们记录的实验数据如表:
实验用品 | 溶液温度 | 中和热 | |||
t1 | t2 | △H | |||
① | 50 mL 0.55 molL﹣1 NaOH溶液 | 50 mL 0.5 molL﹣1 HCl溶液 | 20℃ | 23.3℃ | kJ/mol |
② | 50 mL 0.55 molL﹣1 NaOH溶液 | 50 mL 0.5 molL﹣1 HCl溶液 | 20℃ | 23.5℃ | |
已知:反应后溶液的比热容c为4.18kJ℃﹣1kg﹣1 , 各物质的密度均为1gcm﹣3 . 计算完成上表(保留两位小数).
(4)实验分析 ①若用醋酸代替HCl做实验,测得的中和热的数值(填“偏大”或“偏小”或“无影响”).
②若用60mL 0.5molL﹣1HCl溶液与50mL 0.55molL﹣1NaOH溶液完成实验,与上述实验相比,测得反应放出的热量(填“偏大”或“偏小”或“不变”),中和热(填“偏大”或“偏小”或“不变”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼镁泥主要成分是MgO(占40%),还含有Na2B4O7、CaO、Al2O3、Fe2O3、FeO、MnO、SiO2等杂质。以硼镁泥为原料制取MgSO4·7H2O的工艺流程如下:
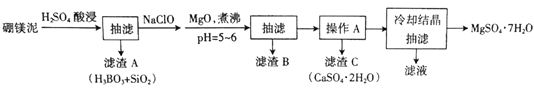
已知部分金属阳离子沉淀的pH:Fe(OH)3:3.2,Al(OH)3:5.2,Fe(OH)2:9.7,Mg(OH)2:11.2。
(1)为提高酸浸时浸出速率,可采取的措施有______________(写出两条)。
(2)H2SO4和Na2B4O7发生反应的化学方程式为________________。
(3)加入NaClO后可以生成一种不溶于水的黑色固体,则反应的离子方程式为_________。
(4)加MgO煮沸,并调整溶液pH=5~6的目的是_______________。
(5)已知MgSO4、CaSO4的溶解度如下表:
| 10℃ | 20℃ | 40℃ | 60℃ |
MgSO4 | 28.2 | 33.7 | 44.5 | 54.6 |
CaSO4 | 0.244 | 0.255 | 0.264 | 0.265 |
“操作A”是将MgSO4和CaSO4混合溶液中的CaSO4。除去,根据上表数据,步骤为________________,__________________。
(6)本实验中多次用到抽滤操作,其装置如图,相比普通过滤,抽滤的优点是____________________。
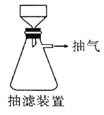
(7)实验中提供的硼镁泥共100g,得到MgSO4·7H2O为172.2g,则MgSO4·7H2O的产率为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:⑴Zn(s)+ ![]() O2(g)=ZnO(s),△H=﹣350kJmol﹣1 , ⑵2Ag(s)+
O2(g)=ZnO(s),△H=﹣350kJmol﹣1 , ⑵2Ag(s)+ ![]() O2(g)=Ag2O(s),△H=﹣25kJmol﹣1 ,
O2(g)=Ag2O(s),△H=﹣25kJmol﹣1 ,
则Zn(s)+Ag2O(s)=ZnO(s)+2Ag(s)的△H等于( )
A.﹣375 kJmol﹣1
B.﹣325 kJmol﹣1
C.+375 kJmol﹣1
D.+325 kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z在元素周期表中的相对位置如下图所示,其中W的最高正价和最低负价的代数和为2。下列判断正确的是( )
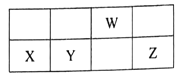
![]()
A. 最高价氧化物对应水化物的酸性:Y>W
B. 最简单气态氢化物的稳定性:Z>Y
C. 元素W与元素Y形成的化合物Y3W4是一种新型有机材料
D. X的单质能与W的最高价氧化物对应水化物的浓溶液反应产生氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作中,符合操作规范的是
A. 洒出的少量酒精在桌面上燃烧起来,立即用湿抹布盖灭
B. 测定溶液的pH,先用水润湿pH试纸,然后将试纸插入待测液中
C. 为了达到节约药品的目的,将实验后剩余的药品放回原瓶
D. 配制稀硫酸时,将水沿量筒壁慢慢注入浓硫酸中,并不断搅拌
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.某温度时,在一个10L恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:

(1)该反应的化学方程式为_________________。
(2)反应开始至2min,以气体X表示的平均反应速率为________________。
(3)平衡时容器内气体的压强与起始时比________________(填“变大”,“变小”或“相等”下同),混合气体的密度与起始时比________________。
(4)将amolX与bmolY的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:n(X)=n(Y)=2n(Z),则原混合气体中a:b=____。
Ⅱ.在恒温恒压的密闭容器中,当下列物理量不再发生交化时:①混合气体的压强;②混合气体的密度;③混合气体的总物质的量;④混合气体的平均相对分子质量;⑤各反应物或生成物的反应速率之比等于化学计量数之比
(1)一定能证明2NO2(g)![]() N2O4(g)达到平衡状态的是________(填序号,下同)。
N2O4(g)达到平衡状态的是________(填序号,下同)。
(2)一定能证明NH2COONH4(s)![]() CO2(g)+2NH3(g)达到平衡状态的是______。
CO2(g)+2NH3(g)达到平衡状态的是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中学教材中常见的金属和非金属元素及其化合物在工业和生活中有重要应用,请回答下列问题:
(1)从海水中提溴是将Cl2:通入浓海水中,生成溴单质,而氯气氧化溴离子是在酸性条件下进行的,其目的是避免__________________。
(2)ClO2是高效、低毒的消毒剂,工业上用KClO3与Na2SO3在H2SO4存在下制得ClO2,该反应氧化剂与还原剂物质的量之比为____。
(3)磷的含氧酸有多种形式,如H3 PO4 、H3PO2(次磷酸)、H3PO3(亚磷酸)等。H3PO3与NaOH反应只生成Na2HPO3和NaH2PO3两种盐,写出H3PO3的第二步电离方程式_________________。H3PO3和碘水反应,棕黄色褪去,再滴加AgNO3溶液,有黄色沉淀生成:请写出H3PO3和碘水反应的化学方程式____。
(4)高铁酸钾(K2FeO4)是一种新型高效水处理剂,其中Fe元素的化合价是____:高铁酸钾溶于水放出氧气,能杀菌消毒,生成能吸附水中悬浮物的物质。用一个离子方程式表示高铁酸钾处理水的过程____。
(5)镁一H2O2酸性燃料电池的反应机理为Mg+H2O2 +2H+==Mg2++2H2O,则正极反应式为________。常温下若起始电解质溶液pH =1,则pH =2时溶液中Mg2+浓度为________。已知Ksp[ Mg(OH)2]=5.6×10 -12,当溶液pH =6时,_____(填“有”或“没有”)Mg( OH)2沉淀。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com