
【题目】下列有关说法不正确的是( )
A.铅蓄电池放电时的负极和正极的质量均增加
B.CaCO3(s)=CaO(s)+CO2(g)在室温下不能自发进行,说明该反应的△H>0
C.对于发应2H2O2![]() 2H2O+O2↑,加入MnO2或升高温度都能加快O2的生成速率
2H2O+O2↑,加入MnO2或升高温度都能加快O2的生成速率
D.H2O与金属Na反应生成1molH2,反应中转移的电子数为6.02×1023
【答案】D
【解析】
A.铅蓄电池在放电过程中,负极电极反应式:Pb+SO42--2e-=PbSO4,负极生成PbSO4质量增加,正极电极反应式为PbO2+4H++SO42-+2e-=PbSO4+2H2O,正极生成PbSO4质量也增加,故A正确;
B.该反应为气体增多的反应,所以△S>0,△H-T△S<0的反应可自发进行,则在室温下不能自发进行,则该反应的△H>0,故B正确;
C.二氧化锰做过氧化氢分解的催化剂,加入二氧化锰能够加快反应速率,升温能够加快任何反应的反应速率,故C正确;
D.H2O与金属Na反应生成1molH2,氢元素化合价由+1价变为0价,转移2mol电子,转移电子数目为2×6.02×1023,故D错误;
故答案为D。


 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数的数值,下列说法正确的是
A. 在标准状况下,11.2L HF含有的分子数目为0.5NA
B. 高温下,16.8 g Fe与足量水蒸气完全反应失去0.8NA个电子
C. 常温下,0.2 L 0.5 mol·L-1 NH4NO3溶液中含有的氮原子数小于0.2NA
D. 18g葡萄糖(C6H12O6)分子含有的羟基数目为0.6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某银白色金属单质A在空气中加热燃烧时发出黄色火焰,得到淡黄色固体B,B和酸性气体D反应能生成C,A露置在空气中足够长时间也会变为C,E与D反应也能生成C,A、B都能与水反应生成E。回答下列问题:
(1)写出下列物质的化学式: B________,C________,D________,E________。
(2)写出下列反应的化学方程式:
①A生成B:____________________;
②B与水反应生成E:________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫代硫酸钠(![]() )可用于照相业作定影剂,也可用于纸浆漂白作脱氯剂等.它易溶于水,难溶于乙醇,受热易分解,在酸性溶液中不能稳定存在.某实验室模拟工业硫化碱法制取硫代硫酸钠,其反应装置及所需试剂如下图:
)可用于照相业作定影剂,也可用于纸浆漂白作脱氯剂等.它易溶于水,难溶于乙醇,受热易分解,在酸性溶液中不能稳定存在.某实验室模拟工业硫化碱法制取硫代硫酸钠,其反应装置及所需试剂如下图:
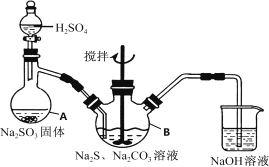
实验具体操作步骤为:
①开启分液漏斗,使硫酸慢慢滴下,适当调节分液的滴速,使反应产生的![]() 气体较均匀地通入
气体较均匀地通入![]() 和
和![]() 的混合溶液中,同时开启电动搅拌器搅动,水浴加热,微沸。
的混合溶液中,同时开启电动搅拌器搅动,水浴加热,微沸。
②直至析出的浑浊不再消失,并控制溶液的![]() 接近7时,停止通入
接近7时,停止通入![]() 气体。
气体。
③趁热过滤,将滤液加热浓缩,冷却析出![]() 。
。
④再经过滤、洗涤、干燥,得到所需的产品。
(1)仪器A的名称是_________。
(2)为了保证硫代硫酸钠的产量,实验中不能让溶液![]() ,请用离子方程式表示原因_________。
,请用离子方程式表示原因_________。
(3)写出三颈烧瓶B中制取![]() 反应的总化学反应方程式_________。
反应的总化学反应方程式_________。
(4)为了验证固体硫代硫酸钠工业产品中含有碳酸钠,选用下列装置进行实验:
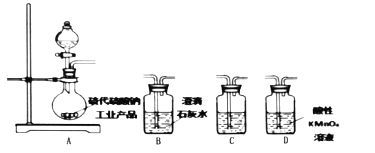
①实验装置的连接顺序依次_________(填装置的字母代号,各装置限用一次),装置C中的试剂为_________。
②能证明固体中含有碳酸钠的实验现象是_________。
③若要检验固体硫代硫酸钠工业产品中含有![]() ,需先加水配成稀溶液,再依次加入的试剂为_________、_________和品红溶液。
,需先加水配成稀溶液,再依次加入的试剂为_________、_________和品红溶液。
(5)![]() 常用作脱氯剂,在溶液中易被
常用作脱氯剂,在溶液中易被![]() 氧化成
氧化成![]() ,该反应的离子方程式为_________。
,该反应的离子方程式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是丁醇的两种同分异构体,其结构简式、沸点及熔点如下表所示:
异丁醇 | 叔丁醇 | |
结构简式 |
|
|
沸点/℃ | 108 | 82.3 |
熔点/℃ | -108 | 25.5 |
下列说法不正确的是
A. 用系统命名法给异丁醇命名为:2-甲基-1-丙醇
B. 异丁醇的核磁共振氢谱有三组峰,且面积之比是1∶2∶6
C. 用蒸馏的方法可将叔丁醇从二者的混合物中分离出来
D. 两种醇发生消去反应后得到同一种烯烃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据元素周期表和元素周期律,下列叙述正确的是( )
A.在周期表金属与非金属分界处寻找用于研制新农药的元素
B.H2、D2、T2互为同位素
C.如图所示实验可证明元素的非金属性:Cl>C>Si
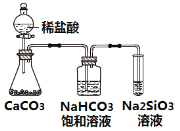
D.用中文“![]() ”(ào)命名的第118号元素在周期表中位于第七周期0族
”(ào)命名的第118号元素在周期表中位于第七周期0族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关硫元素及其化合物的说法或描述正确的是( )
A.硫黄矿制备硫酸经历两步:S![]() SO3
SO3![]() H2SO4
H2SO4
B.酸雨与土壤中的金属氧化物反应后,硫元素以单质的形式进入土壤中
C.在燃煤中加入石灰石可减少SO2排放,发生的反应为2CaCO3+2SO2+O2![]() 2CO2+2CaSO4
2CO2+2CaSO4
D.土壤中的闪锌矿(ZnS)遇到硫酸铜溶液转化为铜蓝(CuS),说明CuS很稳定,不具有还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修5:有机化学基础]
诺氟沙星为喹诺酮类抗生素,其合成路线如下:
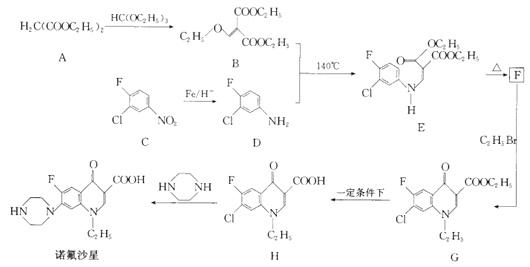
回答下列问题:
(1)化合物A的名称是____________。
(2)诺氟沙星分子中含氧官能团的名称为____________。
(3)C生成D,H生成诺氟沙星的反应类型分别是___________、___________。
(4)F的结构简式为_______________。
(5)G生成H的化学方程式为__________________。
(6)有机物X比B分子少一个CH2原子团,且含有酯基和![]() 结构其中核磁共振氢谱有三组峰,峰面积比为1:3:3的结构简式为__________(任写一种)
结构其中核磁共振氢谱有三组峰,峰面积比为1:3:3的结构简式为__________(任写一种)
(7)参照上述合成路线写出由有机物![]() 、B为有机原料合成
、B为有机原料合成 的路线图______________(无机试剂任选)。
的路线图______________(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“电化学”与人类生产和生活密不可分。
(1)如图为相互串联的甲、乙两个电解池,试回答下列问题。
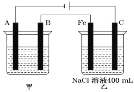
①乙池中若滴入少量酚酞,开始一段时间后,_____电极附近呈红色(填“铁”或“碳”)。
②甲池若为用电解原理精炼铜的装置,A极电极反应式为_____。
③甲池若为用电解原理精炼铜的装置,阴极增重12.8g时,则乙池阳极放出气体在标准状况下的体积为_____(不考虑气体溶解情况)。
(2)人工肾脏可用电化学方法除去代谢产物中的尿素[CO(NH2)2],原理如图。
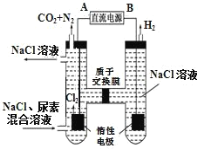
①阳极反应生成的氯气将尿素氧化而得以除去,试写出该反应的化学方程式_____。
②若两极共收集到气体13.44L(标况),则除去的尿素质量为_____ g(忽略气体的溶解)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com