
| ��c |
| ��t |
| 0.4mol/L |
| 2s |
| 0.2mol/L |
| 2s |
| 0.4 |
| 1 |
| 0.2 |
| 0.5 |


 ��ĩ1�����ʽ���������ϵ�д�
��ĩ1�����ʽ���������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
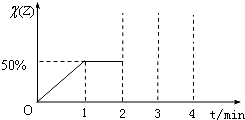
��3��ʵ�������£��ֱ����ݻ�Ϊ2L�ĺ����ܱ������г���2mol A��1mol B��������Ӧ2A��g��+B��g��?2D��g����H=-Q kJ?mol-1��������������������ʾ��
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
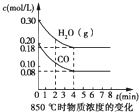 ij�о�С�����÷�ӦCO��g��+H2O��g��?CO2��g��+2H2��g����H=-41.2kJ/mol���Ʊ�CO2��H2�Ļ�����壬����һ���о�CO2��H2�Բ�ͬ�����֮�Ȼ��ʱ�ں��������µķ�Ӧ�������ش��������⣺
ij�о�С�����÷�ӦCO��g��+H2O��g��?CO2��g��+2H2��g����H=-41.2kJ/mol���Ʊ�CO2��H2�Ļ�����壬����һ���о�CO2��H2�Բ�ͬ�����֮�Ȼ��ʱ�ں��������µķ�Ӧ�������ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014ѧ��ɽ��ʡ�Ͳ��и���3��ģ�⿼�����ۻ�ѧ�Ծ��������棩 ���ͣ������
��Ļ������������Ϳ����з�������Ҫ������
��1��SO2Cl2����������ҽҩƷ��Ⱦ�ϡ�������Լ��ȡ���֪��SO2Cl2(g) SO2(g)��Cl2(g)? ��H����97.3 kJ��mol��1��ij�¶�ʱ�����Ϊ1 L�ĺ����ܱ������г���0. 20mol SO2Cl2���ﵽƽ��ʱ�������к�0.18mol SO2����˹��̷�Ӧ���յ�����Ϊ_____kJ�����¶�ʱ��Ӧ��ƽ�ⳣ��Ϊ_____�����������û��������������BaCl2��Һ�У��������ɳ���������Ϊ_______��
SO2(g)��Cl2(g)? ��H����97.3 kJ��mol��1��ij�¶�ʱ�����Ϊ1 L�ĺ����ܱ������г���0. 20mol SO2Cl2���ﵽƽ��ʱ�������к�0.18mol SO2����˹��̷�Ӧ���յ�����Ϊ_____kJ�����¶�ʱ��Ӧ��ƽ�ⳣ��Ϊ_____�����������û��������������BaCl2��Һ�У��������ɳ���������Ϊ_______��
��2����ҵ���Ʊ�����Ĺ����д��ڷ�Ӧ��2SO2(g)��O2(g) 2SO3(g) ��H����198kJ��mol��1400����1.01��105Pa�����ݻ�Ϊ2L�ĺ����ܱ������г���һ���� SO2��O2��n(SO3)��n(O2)��ʱ��ı仯������ͼ��ʾ��
2SO3(g) ��H����198kJ��mol��1400����1.01��105Pa�����ݻ�Ϊ2L�ĺ����ܱ������г���һ���� SO2��O2��n(SO3)��n(O2)��ʱ��ı仯������ͼ��ʾ��
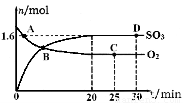
��0��20min��Ӧ��ƽ��������(O2)��___________��
������������ȷ����???????? ��
a��A������(SO2)������(SO2)
b��B�㴦��ƽ��״̬
c��C���D��n(SO2)��ͬ
d�������������䣬500��ʱ��Ӧ��ƽ�⣬n(SO3)��ͼ��D���ֵ��
��3����ҵ����Na2SO3��Һ���������е�SO2��������ͨ��1.0 mol��L��1��Na2SO3��Һ������ҺpHԼΪ6ʱ��Na2SO3��Һ����SO2�����������½���Ӧ�������ռ�����ʱ��Һ��c (SO32��)��Ũ����0.2 mol��L��1������Һ��c(HSO3��)��_________mol��L��1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013���Ĵ�ʡ�߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�ں��º��������£����ݻ�Ϊ2L���ܱ������г���2.0molSO2��2.0molO2����֪��2SO2(g)��O2(g) 2SO3(g) ∆H=-akJ/mol��a>0������2min�ﵽƽ��״̬����Ӧ����0.25akJ�������ж���ȷ����
2SO3(g) ∆H=-akJ/mol��a>0������2min�ﵽƽ��״̬����Ӧ����0.25akJ�������ж���ȷ����
A����1minʱ��c��SO3��+c��SO2��=1.0 mol��L��1
B����2min�ڣ�v��SO2��=0.25 mol��L��1��min-1
C�����ٳ���2molSO3���ﵽƽ��ʱSO3������������С
D����Ӧ������ͬ������ʼʱ��Ӧ��������2molSO3���ﵽƽ��ʱ��Ӧ����0.75 akJ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com