
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NaCl(aq)+ AgNO3(aq)= AgCl(s)+ NaNO3(aq )△H<0 |
| B.2CH3OH (l) +3O2(g) = 2CO2(g) + 4H2O (l)△H<0 |
| C.2FeCl3(aq)+Fe(s) = 3FeCl3(aq)△H < 0 |
| D.2H2 (g) + O2 (g) = 2H2O (l)△H < 0 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.通入氧气的一极是负极 |
| B.放电时,溶液中的OH-向正极移动 |
| C.反应中若有6mol电子发生转移,则有32g CH3 OH被还原 |
| D.该电池工作时甲醇一极附近溶液的pH降低 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.正极附近的SO4 2- 离子浓度逐渐增大 | B.铜片上有H2逸出 |
| C.溶液的pH逐渐变小 | D.电子通过导线由铜片流向锌片 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.若a极是铜,b极为铁时,当电池消耗1.6g O2,b极上析出6.4g铜 |
| B.燃料电池工作时,正极反应为:O2 + 2H2O + 4e-= 4OH- |
| C.若a极是粗铜,b极是纯铜时,a极减少的质量等于b极上析出铜的质量。 |
| D.若a、b两极均是石墨时,b极反应为4OH- - 4e-=O2↑+ 2H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
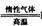 Li2FeSiO4 +Li2SO4 +SiO2
Li2FeSiO4 +Li2SO4 +SiO2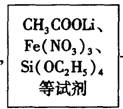
 Li2FeSiO4
Li2FeSiO4 Li2FeSiO4则该电池的负极是____ ;充电时,阳极反应的电极反应式为 ;
Li2FeSiO4则该电池的负极是____ ;充电时,阳极反应的电极反应式为 ;查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.正极反应为:Zn—2e-=Zn2+ |
| B.电池反应为:Zn+Cu2+=Zn2+ +Cu |
| C.在外电路中,电子从正极流向负极 |
| D.盐桥中的K+移向ZnSO4溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com