
(8分)下图中每一方框代表一种反应物或生成物:
(1)若X由M、N两种短周期且同周期元素组成,M原子的最外层电子数比最内层电子数少1,N元素最高正价与它的最低负价代数和为6。反应④的数据如表格所示且D、G在常温下均为气体。
| | C | D | G |
| 起始 | 3 mol | 1 mol | 0 |
| 3 min时 | 2.4 mol | 0.8 mol | 0.4 mol |
(1)Cl2+2OH-===Cl-+ClO-+H2O
c(Cl-)>c(NH)>c(H+)>c(OH-)
(2)2CuSO4+2H2O 2Cu+2H2SO4+O2↑
2Cu+2H2SO4+O2↑
S(s)+O2(g)= SO2(g);ΔH=-297.6 kJ·mol-1
解析试题分析:由转换过程可推知X为NaCl; A为NaOH;B为Cl2;C为H2;F为HCl;E为NaClO;D为N2;G为NH3。
(1)①反应②为氯气与氢氧化钠溶液的反应,其离子方程式为Cl2+2OH-===Cl-+ClO-+H2O
②物质G与F反应所形成盐的化学式为NH4Cl,由于NH4+的水解,因此溶液中各离子的浓度大小为c(Cl-)>c(NH)>c(H+)>c(OH-)。
(2)“若X是一种含氧酸盐,B是金属单质,C、D是非金属单质”则X为CuSO4,因此反应①的化学方程式为:2CuSO4+2H2O2Cu+2H2SO4+O2↑。固态D为S单质,“1 g固态D在C中完全反应放出9.3 kJ的热量”,设1mol S反应放出的热量为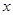 ,可得关系式
,可得关系式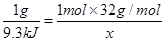 ,解得
,解得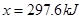 。因此该热化学方程式为:
。因此该热化学方程式为:
S(s)+O2(g)= SO2(g);ΔH=-297.6 kJ·mol-1
考点:电解;离子浓度大小比较;热化学方程式的书写;元素周期表
点评:此题较为综合,考查的知识点较多,属于中档题。对于此类题型,是高考命题的重点。对于离子浓度大小的比较,应注意考虑溶液中离子的水解与电离;热化学方程式的书写应注意化学反应热的计算,尤其是盖斯定律的应用。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
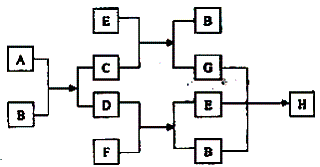
已知气态烃D(其密度在同温同压下是氢气密度的13倍)跟物质F反应时产生明亮而带浓烈黑烟的火焰。请写出下列字母代表的物质的化学式(分子式):A 、B 、D 、E 、H 。
查看答案和解析>>
科目:高中化学 来源: 题型:

已知气态烃D(其密度在同温同压下是氢气密度的13倍)跟物质F反应时产生明亮而带浓烈黑烟的火焰。请写出下列字母代表的物质的化学式(分子式):A_____________、B_____________、D_____________、E_____________、H_____________。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年河南省镇平一高高二第一次月考化学试卷(带解析) 题型:填空题
(10分)下图中每一方框中的字母代表一种反应物或生成物。已知:A、B、C、D均为前三周期元素的单质,也是中学化学教材中常见的物质。其中A、B为固体,且B是良好的半导体材料,C、D为气体,电解H的饱和溶液生成x、C和D,此反应是一个重要的化工反应(物质间相互转化时参加反应或生成的H2O已略去)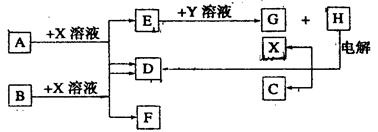
(1)B单质为 .列举B的氧化物的一种重要的工业用途为 。
(2)X的电子式为 ,Y是(填化学式) 。
(3)E和G在水溶液中混合反应,其离子反应方程式为
。
若在E的水溶液中通入过量的CO2,其离子反应方程式为
。
(4)25℃时用石墨电极电解含0.2 mol H的水溶液,在阳极产生0.2 mol气体时,测得此时溶液的体积为200 mL,则该溶液中C(OH-)最接近的数值为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
(08山东临沂质检) (10分)下图中每一方框代表一种反应物或生成物

(1)若X由 M、N两种短周期且同周期元素组成,M原子的最外层电子数是最内层电子数的![]() ,N元素最高正价与它的负价代数和为6。反应④的数据如右上表格所示。
,N元素最高正价与它的负价代数和为6。反应④的数据如右上表格所示。
①写出反应②的离子方程式 。
②物质 G 的水溶液中离子浓度由大到小的顺序为 。
(2)若X是一种含氧酸盐,且B是一种过渡元素的金属,反应①所得B、C的物质的量之比为4:1,反应②不需特定的反应条件就能进行,且A的浓度不同,产物E不同,则X物质的化学式可能是 。
(3) 若X是一种含氧酸盐,B 是金属单质,C、D是非金属单质,反应②需要B与A的浓溶液共热才能进行,且生成的E与G是同一种物质。写出反应①的化学方程式 。1g 固态 D 在 C 中完全反应放出 9.3kJ 的热量 , 写出该反应的热化学方程式_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com