
【题目】实验室在加热条件下H2还原CuO所得的红色固体可能是Cu与Cu2O的混合物,已知Cu2O在酸性溶液中可发生自身氧化还原反应,生成Cu2+和单质铜。现有8g CuO被H2还原后,得到红色固体6.8g。
(1)写出H2还原CuO生成Cu2O的化学方程式 ;
(2)6.8 g上述混合物中含Cu与Cu2O的物质的量之比是 ;
(3)若将6.8 g上述混合物与足量的稀硫酸充分反应后过滤,可得到固体 g
【答案】(1)H2+2CuO![]() Cu2O+H2O
Cu2O+H2O
(2)2︰1(3)4.8
【解析】
试题分析:(1)依据题意CuO被H2还原生成Cu2O和水,该反应的化学方程式为:H2+2CuO![]() Cu2O+H2O。
Cu2O+H2O。
(2)n(CuO)=8g÷80g/mol==0.1mol,根据Cu、O原子守恒得n(O)=n(CuO)═n(Cu)=0.1mol;固体由CuO生成Cu和Cu2O,减少的质量为氧元素的质量,即8g-6.8g=1.2g,减少的n(O)=1.2g÷16g/mol=0.075mol,所以Cu2O中n(O)=0.1mol-0.075mol=0.025mol,所以n(Cu2O)=0.025mol,根据铜元素守恒得n(Cu)=0.1mol-2×0.025mol=0.05mol,所以n(Cu)与n(Cu2O)之比是2:1。
(3)n(Cu)=0.1mol-2×0.025mol=0.05mol,
所以m(Cu)=0.05mol×64g/mol=3.2g,
m(Cu2O)=6.8g-3.2g=3.6g。Cu2O和稀硫酸反应,铜和稀硫酸不反应,
设Cu2O和稀硫酸反应生成铜的质量为x,氧化亚铜和稀硫酸反应的方程式为:
Cu2O+H2SO4=CuSO4+Cu+H2O
144g 64g
3.6g x
144g:64g=3.6g:x
x=1.6g
所以可得到固体的质量=3.2g+1.6g=4.8g。
故答案为:4.8。


科目:高中化学 来源: 题型:
【题目】足量的铜溶于一定量浓HNO3中,产生NO、N2O4 NO2的混合气体,这些气体若与1.12 LO2(标准状况)混合后通入水中,气体被水完全吸收。若向原所得溶液中加入5mol.L的H2SO4溶液100mL,则继续溶解的铜的质量
A.6.4g B.9.6g C.19.2g D.24g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图装置中发生反应的离子方程式为:Zn+2H+=Zn2++H2↑,下列说法错误的是
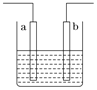
A. a、b不可能是同种材料的电极
B. 该装置可能是电解池,电解质溶液为稀盐酸
C. 该装置可能是原电池,电解质溶液为稀盐酸
D. 该装置可看作是铜-锌原电池,电解质溶液是稀硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2-氯丁烷常用于有机合成等,有关2-氯丁烷的叙述正确的是
A.分子式为C4H8Cl2
B.与硝酸银溶液混合产生不溶于稀硝酸的白色沉淀
C.微溶于水,可混溶于乙醇、乙醚、氯仿等多数有机溶剂
D.与氢氧化钠、乙醇在加热条件下的消去反应有机产物只有一种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将如图所示实验装置的K闭合,下列判断正确的是( )
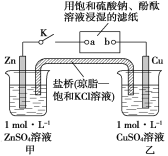
A.电子沿Zn→a→b→Cu路径流动
B.Cu电极上发生还原反应
C.片刻后甲池中c(SO![]() )增大
)增大
D.片刻后可观察到滤纸b点变红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将A和B加入密闭容器中,在一定条件下发生反应:A(g)+B(s)![]() 2C(g),忽略固体体积,平衡时C的体积分数(%)随温度和压强的变化如下表所示:
2C(g),忽略固体体积,平衡时C的体积分数(%)随温度和压强的变化如下表所示:
压强/MPa 体积分数/% 温度/℃ | 1.0 | 2.0 | 3.0 |
800 | 54.0 | a | b |
900 | c | 75.0 | d |
1000 | e | f | 83.0 |
①a﹤b ②该反应的熵变△S﹤0 ③900℃、2.0MPa时A的转化率为60%
④K(1000℃)﹥K(800℃) ⑤正反应为吸热反应 上述①~⑤中正确的有( )
A.4个 B.3个 C.2个 D.1个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知热化学方程式:2SO2(g)+ O2(g) ![]() 2 SO3(g) △ H = ―198kJ/mol,下列说法正确的是( )
2 SO3(g) △ H = ―198kJ/mol,下列说法正确的是( )
A.2 L SO3气体分解成1 L O2与2 L SO2吸收198 kJ热量
B.1 mol O2与2 mol SO2混合,生成气态SO3放出的热量等于198 kJ
C .1个O2分子与2个SO2分子反应生成2个SO3气体分子放出198 kJ热量
D.在相同条件下,1 mol O2与2 mol SO2的能量总和大于2 mol SO3气体的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为2升的密闭容器中,有反应mA(g)+nB(g)![]() pC(g)+qD(g),经过5分钟达到平衡,此时,各物质的变化为A减少了a mol·L-1,B的平均反应速度VB=a/15mol·L-1·min-1,C增加了2a/3 mol·L-1,这时若增加系统压强,发现A与C的百分含量不变,则m︰n︰p︰q为( )
pC(g)+qD(g),经过5分钟达到平衡,此时,各物质的变化为A减少了a mol·L-1,B的平均反应速度VB=a/15mol·L-1·min-1,C增加了2a/3 mol·L-1,这时若增加系统压强,发现A与C的百分含量不变,则m︰n︰p︰q为( )
A.1︰1︰1︰1 B.1︰3︰2︰2 C.1︰3︰2︰1 D.3︰1︰2︰2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com