
(10分)有10 mL NaOH溶液,向其中通人一定量的CO2,得到了Na2CO3和NaHCO3的混合溶液。向所得溶液中逐滴加入0.1 mol/L的盐酸,边加边振荡。使其充分反应,产生CO2气体的体积(标准状况)与所加盐酸体积之间的关系如下图所示。
请回答下列问题:
(1)向Na2CO3和NaHCO3的混合溶液中滴加盐酸时发生反应的离子方程式为 、 。
(2)混合溶液中Na2CO3和NaHCO3的物质的量之比为 。
(3)原NaOH溶液中NaOH的物质的量浓度为 ,所通CO2气体的体积在标准状况下为 。
(4)a mL同浓度的NaOH溶液,与足量的CO2发生反应,得到的溶液中所含溶质的最大质量为 (用含a的数学式表示)。
 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源:2012届江西省红色六校高三第一次联考化学试卷 题型:实验题
(10分)8.34gFeS04·7H20样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如下图所示。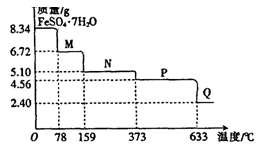
请回答下列问题:
(1)试确定78℃时固体物质M的化学式: 。
(2)取适量380℃时所得的样品P,隔绝空气加热至650℃,得到一种固体物质Q,同时有两种无色气体生成,写出该反应的化学方程式
(3)某兴趣小组用如图所示装置设计实验,验证(2)中生成的气态物质,并测定已分解的P的质量(不考虑装置内空气的影响)。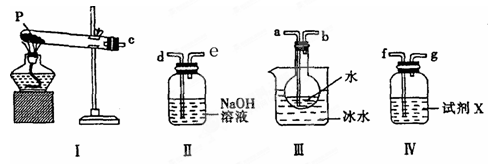
①试剂X的名称是 。
②按气流方向连接各仪器,用字母表示接口的连接顺序:c→ 。
③充分反应后,利用装置III中圆底烧瓶内混合物测定已分解的P的质量,其操作步骤为:第一步:向圆底烧瓶中逐滴加入氯化钡溶液,直至沉淀完全;第二步:过滤混合物,在过滤器上将沉淀洗净后,烘干并冷却至室温,称重。第三步:继续烘干、冷却并称量直至连续两次称量的质量差不超过0.1g为止。若最终得到沉淀的质量为Wg,则已分解的P的质量 (填计算式) 。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年陕西省宝鸡中学高一下学期期末考试化学试卷(带解析) 题型:计算题
(10分计入总分)在一个容积固定的反应器中,有一可左右滑动的密封隔板,两侧分别进行如下图的反应,各物质量起始加入量如下:M为2.5moL,N为3mol,P为0 mol。A、C、D各为0.5mol, B为Xmol,当X在一定范围内变化时,均可以调节反应器的温度,使两侧面反应达平衡,并且隔板刚处于中间位置。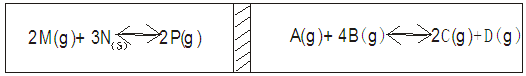
若达平衡后,测得M的转化率为75%,请读写下列空白。
①达平衡后,反应左室气体总的物质的量为 。
②若欲使右室V正>V逆,X的取值范围是 。
③若欲使右室反应V逆>V正,X的取值范围是 。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年江西省红色六校高三第一次联考化学试卷 题型:实验题
(10分)8.34gFeS04·7H20样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如下图所示。

请回答下列问题:
(1)试确定78℃时固体物质M的化学式: 。
(2)取适量380℃时所得的样品P,隔绝空气加热至650℃,得到一种固体物质Q,同时有两种无色气体生成,写出该反应的化学方程式
(3)某兴趣小组用如图所示装置设计实验,验证(2)中生成的气态物质,并测定已分解的P的质量(不考虑装置内空气的影响)。

①试剂X的名称是 。
②按气流方向连接各仪器,用字母表示接口的连接顺序:c→ 。
③充分反应后,利用装置III中圆底烧瓶内混合物测定已分解的P的质量,其操作步骤为:第一步:向圆底烧瓶中逐滴加入氯化钡溶液,直至沉淀完全;第二步:过滤混合物,在过滤器上将沉淀洗净后,烘干并冷却至室温,称重。第三步:继续烘干、冷却并称量直至连续两次称量的质量差不超过0.1g为止。若最终得到沉淀的质量为Wg,则已分解的P的质量 (填计算式) 。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年北京四中高三上学期期中测试化学试卷 题型:填空题
(10分)X、Y、Z、M、R、Q是短周期主族元素,部分信息如下表所示:
|
|
X |
Y |
Z |
M |
R |
Q |
|
原子半径/nm |
|
|
0.186 |
0.074 |
0.099 |
0.143 |
|
主要化合价 |
|
-4,+4 |
|
-2 |
-1,+7 |
+3 |
|
其它 |
阳离子核外无电子 |
无机非金属材料的主角 |
焰色反应呈黄色 |
|
|
|
(1)R在元素周期表中的位置是________________ ;R在自然界中有质量数为35和37的两种核素,它们之间的关系互为________________ 。
(2)Z的单质与水反应的离子方程式是__________________________________ 。
(3)根据表中数据推测,Y的原子半径的最小范围是________________ 。
(4)Z、M、Q的简单离子的离子半径的大小顺序为________________ 。
(5)Y与R相比,非金属性较强的是________________(用元素符号表示),下列事实能证明这一结论的是________________(选填字母序号)。
a. 常温下Y的单质呈固态,R的单质呈气态
b. 稳定性XR >YX4
c. Y与R形成的化合物中Y呈正价
(6)甲、乙是上述部分元素的最高价氧化物的水化物,且甲 + 乙→丙 + 水 。若丙的水溶液呈碱性,则丙的化学式是________________________________________。
(7)Y的单质能和Z的最高价氧化物的水化物的水溶液发生反应,生成相同条件下密度最小的气体。请写出该反应的化学方程式_____________________________________。
查看答案和解析>>
科目:高中化学 来源:2010年浙江省杭州地区七校联考高二第二学期期中化学试卷 题型:实验题
(10分)实验小组测定某肥料中的总氮含量(以氮的质量分数表示) ,实验装置如下图(图中加热及夹持仪器略去):

称取1.200 g样品,通过化学方法将肥料中的氮转化成铵盐(除样品外,所加试剂均不含氮元素),然后在碱性溶液中蒸馏氨,用25.00 mL浓度为0.5000 mol/L-1硫酸溶液充分吸收,再用浓度为0.1000 mol/L-1氢氧化钠溶液滴定未反应的硫酸。重复上述实验三次。实验数据如下:
|
实验次数 |
氢氧化钠溶液的体积 |
|
|
滴定前刻度(mL) |
滴定后刻度(mL) |
|
|
1 |
0.00 |
5. 01 |
|
2 |
6.00 |
10.99 |
|
3 |
12.00 |
17.60 |
(1)写出圆底烧瓶内发生反应的离子方程式 。
(2)分液漏斗和圆底烧瓶之间的导管a的作用是 ; b的作用是
;冷凝管中从(填“n”或“m”) 口进水。
(3)在滴定过程中,以下操作会使所测总氮含量偏小的是(填序号) 。
A.锥形瓶水洗后未烘干 B.滴定过程中滴定管有漏水现象
C.滴定过程中有少量溶液从锥形瓶中溅出 D.滴定前滴定管内有气泡,滴定后没有了
(4)若实验操作均正确,但测定结果偏低,可能造成该结果的主要原因是 。
(5)利用题目中所给数据计算肥料中总氮含量为 %(计算结果保留到小数点后1位)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com