
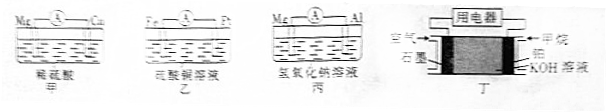
| 装置序号 | 负极 | 阳离子移向 (填电极材料名称) |
| 甲 | ||
| 乙 | . |
分析 电池甲:在稀硫酸中,镁比铝活泼,镁为负极,发生氧化反应,铝为正极,H+在铝极上发生还原反应;
乙电池:铁比铂活泼,铁为负极;
丙电池:在氢氧化钠溶液中,铝与NaOH溶液反应,铝失去电子,发生氧化反应,铝离子与氢氧化钠反应生成偏铝酸根离子和水;
丁电池:是燃料电池,甲烷与氧气反应,甲烷发生氧化反应,在碱中生成碳酸盐和水,氧气发生还原反应.所以,在负极区通入甲烷,在正极区通入空气,以此解答该题.
解答 解:(1)甲中镁比铝活泼,镁为负极,铝为正极,原电池工作时阳离子向铝极移动;
乙中铁为负极,铂为正极,阳离子向铂电极移动,
故答案为:
| 装置序号 | 负极 | 阳离子移向 (填电极材料名称) |
| 甲 | Mg | Al |
| 乙 | Fe | Pt |
点评 本题考查了氧化还原反应、原电池的工作原理的应用、电极反应式的书写等,题目难度中等,熟悉氧化还原反应的规律、原电池的工作原理是解题关键,注意培养阅读材料获取信息的能力.


科目:高中化学 来源: 题型:解答题
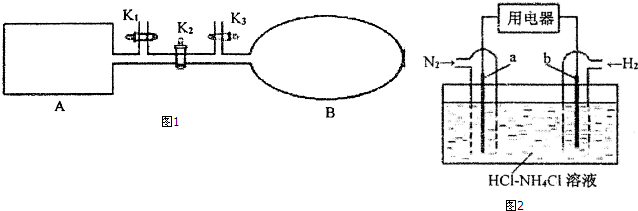
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Si投入NaOH溶液中Si+2OH-═SiO${\;}_{3}^{2-}$+H2 | |
| B. | 把Al中投入到少量氢氧化钠溶液Al3++3OH-═Al(OH)3↓ | |
| C. | 向明矾水溶液中滴加氢氧化钡溶液,恰好使“SO42-”完全沉淀:Al3++2SO42-+2Ba2++2OH-═2BaSO4↓+Al(OH)3 | |
| D. | Na[Al(OH)4]溶液中加入过量的CO2:[Al(OH)4]-+CO2═HCO${\;}_{3}^{-}$+Al(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
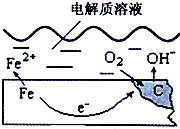 如图是钢铁在潮湿空气里发生电化学腐蚀原理示意图,发生的反应为:
如图是钢铁在潮湿空气里发生电化学腐蚀原理示意图,发生的反应为:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 18gH20中含有的中子数为10NA | |
| B. | 6.4g铜完全溶解于一定浓度的硝酸时,转移的电子数为0.2NA | |
| C. | 1L0.1mol/L的Na2CO3溶液中,离子总数为0.3NA | |
| D. | 在密闭容器中,2HI(g)?H2(g)+I2(g)△H=+14.9kJ•mol-1,若投入NA个HI分子,反应平衡时,吸热7.45kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Q1=$\frac{1}{2}$Q | B. | Q1<$\frac{1}{2}$Q | C. | Q1>$\frac{1}{2}$Q | D. | Q1=Q |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市高二上9月调研化学试卷(解析版) 题型:实验题
某实验小组用0.50 mol·L-1NaOH溶液和0.50 mol·L-1硫酸溶液进行中和热的测定。
Ⅰ.配制0.50 mol·L-1NaOH溶液
(1)若实验中大约要使用245mLNaOH溶液,至少需要称量NaOH固体 g。
(2)从下图中选择称量NaOH固体所需要的仪器是(填字母): 。
名称 | 托盘天平 (带砝码) | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
仪器 |
|
|
|
|
|
|
序号 | a | b | c | d | e | f |
Ⅱ.测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示。
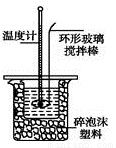
(1)不能用铜丝搅拌棒代替环形玻璃搅拌棒的理由是 。
(2)在操作正确的前提下,提高中和热测定准确性的关键是_____________。大烧杯如不盖硬纸板,求得的中和热数值将 (填“偏大”、“偏小”或“无影响”)。结合日常生活实际该实验在 中(家用产品)效果更好。
(3)写出该反应中和热的热化学方程式:(中和热为57.3 kJ·mol-1) 。
(4)取50 mLNa OH溶液和30 mL硫酸溶液进行实验,实验数据如下表。
OH溶液和30 mL硫酸溶液进行实验,实验数据如下表。
试验次数 | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 29.6 | |
2 | 27.0 | 27.4 | 27.2 | 31.2 | |
3 | 25.9 | 25.9 | 25.9 | 29.8 | |
4 | 26.4 | 26.2 | 26.3 | 30.4 | |
①表中的温度差平均值为 ℃。
②近似认为0.50 mol·L-1 NaOH溶液和0.50 mol·L-1硫酸溶液的密度都是1 g·cm-3,中和后生成溶液的比热容c = 4.18 J·(g·℃)-1。则中和热ΔH= (取小数点后一位)。
③上述实验数值结果与57.3 kJ·mol-1有偏差,产生偏差的原因可能是(填字母) 。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
④实验中改用60mL0.5mol/L盐酸跟50mL0.55 mol·L-1氢氧化钠进行反应,与上述实验相比,所放出的热量 (填相等或不相等,下同),所求的中和热无偏差时 简述理由 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西省高一上第一次月考化学卷(解析版) 题型:选择题
质量相等的下列物质中,含分子数最多的是
A.CH4 B.O2 C.NH3 D.CO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com