

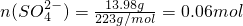 ,
, =0.18 mol,
=0.18 mol,

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:江苏省南京市白下区2011届高三二模化学试题 题型:058
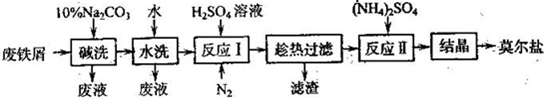
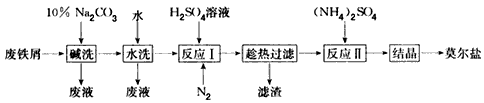
“废铁屑为原料生产莫尔盐的主要流程如下:
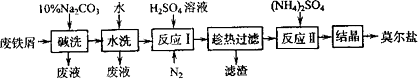
(1)“反应Ⅰ”中通入N2的作用是________________.
(2)称取23.52 g新制莫尔盐,溶于水配制成100 mL溶液,将所得溶分成两等份.一份加入足量Ba(OH)2溶液,并微热,逸出能使湿润的红色石蕊试纸变蓝的气体,同时生成白色沉淀,随即沉淀变为灰绿色,最后带有红褐色;用足量稀盐酸处理沉淀物,充分反应后过滤、洗涤和干燥,得白色固体13.98 g.另一份用0.2000 mol·L-1 K2Cr2O7酸性溶液滴定,当Cr2O![]() 恰好完全被还原为Cr3+时,消耗K2Cr2O7溶液的体积为25.00 mL.通过计算确定莫尔盐的化学式________.
恰好完全被还原为Cr3+时,消耗K2Cr2O7溶液的体积为25.00 mL.通过计算确定莫尔盐的化学式________.
(3)若将“水洗”这一步去掉,则所得产品中SO![]() 的质量分数会________(填“偏大”、“偏小”或“不变”).
的质量分数会________(填“偏大”、“偏小”或“不变”).
查看答案和解析>>
科目:高中化学 来源:江苏模拟题 题型:填空题
查看答案和解析>>
科目:高中化学 来源:2011年江苏省南京市高考化学二模试卷(解析版) 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com