
【化学-选修5有机化学基础】
(1)乙基香草醛 是食品添加剂的增香原料,其香味比香草醛更浓郁。写出乙基香草醛分子中两种含氧官能团的名称 、 ,核磁共振氢谱显示该分子中有 种不同类型的氢原子。
是食品添加剂的增香原料,其香味比香草醛更浓郁。写出乙基香草醛分子中两种含氧官能团的名称 、 ,核磁共振氢谱显示该分子中有 种不同类型的氢原子。
(2)乙基香草醛的同分异构体A是一种有机酸,A可发生以下变化:

已知:a.RCH2OH RCHO
RCHO
b.与苯环直接相连的碳原子上有氢时,此碳原子才可被酸性KMnO4溶液氧化为羧基。
①由A→C的反应方程式_______________________,属于______(填反应类型)。
②B的结构简式为______________________。
③写出在加热条件下C与NaOH醇溶液发生反应的化学方程式______________________。
(3)乙基香草醛的另一种同分异构体D( )是一种医药中间体,请设计合理方案用茴香醛(
)是一种医药中间体,请设计合理方案用茴香醛( )合成D。(其他原料自选,用反应流程图表示并注明必要的反应条件).
)合成D。(其他原料自选,用反应流程图表示并注明必要的反应条件).
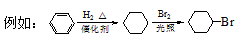
_______________________________
(3)乙基香草醛的同分异构体有很多种,满足下列条件的同分异构体有______种,其中有一种同分异构体的核磁共振氢谱中出现4组峰,吸收峰的面积之比为1:1:2:6,该同分异构体的结构简式为______.
①能与NaHCO3溶液反应
②遇FeCl3溶液显紫色,且能与浓溴水反应
③苯环上有两个烃基
④苯环上的官能团处于对位
(1)醛基、酚羟基、醚键(答出其中的2种即可);7;(2)① ,取代反应; ②
,取代反应; ② ;③
;③
(3)
(4)3 ,  。
。
【解析】
试题分析:(1)根据乙基香草醛的结构简式,得出含有的含氧官能团:醛基、酚羟基、醚碱,苯环上有3种、醛基上1种、酚羟基上1种、乙基上2种,核磁共振氢谱有7种不同的氢原子;(2)A是有机酸,存在-COOH,A→B在CrO3/H2SO4,B能发生银镜反应,说明A中存在-CH2OH,A被酸性高锰酸钾氧化成苯甲酸,说明与苯环直接相连的碳原子上有氢,同时苯环上只有一种取代基,对比A、C的化学式,A→C:Br取代了羟基的位置,说明A中含有-OH,综上所述A的结构简式: ,①A→C,对比化学式C比A少了一个-OH,C比A多了一个Br,说明HBr的Br取代A中-OH,发生的取代反应,反应方程式:
,①A→C,对比化学式C比A少了一个-OH,C比A多了一个Br,说明HBr的Br取代A中-OH,发生的取代反应,反应方程式: +HBr→
+HBr→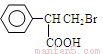 +H2O;②根据RCH2OH
+H2O;②根据RCH2OH RCHO ,得出B的结
RCHO ,得出B的结 构简式:
构简式: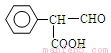 ;③C的结构简式中含有-Br能在NaOH的醇溶液中发生消去反应,-COOH与NaOH发生中和反应,反应方程式:
;③C的结构简式中含有-Br能在NaOH的醇溶液中发生消去反应,-COOH与NaOH发生中和反应,反应方程式:
(3)D: 是由
是由 和CH3OH发生酯化反应得到,
和CH3OH发生酯化反应得到, 变成
变成 ,
,
路线: ;
;
(3)①能与NaHCO3反应,结构中有-COOH,②遇FeCl3溶液显紫色,含有酚羟基,且能与浓溴水反应,说明酚羟基邻位或对位上有氢,③苯环上有两个烃基,说明苯环上有个4个取代基,④苯环上官能团的位置是对位,-OH、-COOH是对位,符合以上的结构简式:
核磁共振氢谱出现4种峰,说明有4种不同的氢原子,吸收峰的面积之比为1:1:2:6,说明四种氢的个数1:1:2:6,上述三种结构简式中不同氢的个数比分别是:1:1:2:6、1:1:1:1:6、1:1:1:1:6,符合题意是 。
。
考点:考查有机物的推断、官能团、氢原子的种类、化学反应方程式的书写,同分异构体的书写等相关知识。
考点分析: 考点1:有机化学知识综合应用 考点2:有机化合物的分类、命名与结构特点 试题属性

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014-2015学年湖北省稳派教育高三一轮复习质量检测理科综合化学试卷(解析版) 题型:实验题
某同学设计如图所示装置(夹持装置已略去,量气管可上下移动)可分别进行下列实验探究

实验 | 药品 | 制取气体 | 量气管中液体 |
Ⅰ | 铜片,浓HNO3(过量) | NO2 | CCl4 |
Ⅱ | NH3 | 煤油 | |
Ⅲ | MnO2,HCl(浓) | Cl2 | |
Ⅳ | 硅铁合金,NaOH溶液 | H2 | H2O |
请回答下列问题:
(1)实验前,某同学检查装置气密性的操作方法是:将活塞K关闭,再将量气管向上提高,其判断装置漏气或不漏气的现象分别是_____
(2)另一同学欲通过实验Ⅰ收集并测量NO2气体的体积来探究铜片的纯度,所测得的结果比真实值偏小(不考虑操作误差),你认为可能的原因是____。
(3)若进行实验II制NH3,则烧瓶和分液漏斗中应分别盛装适量的____。
(4)若进行实验III,该装置缺少的玻璃仪器是____;该反应的离子方程式是_________ 量气管中最好装的液体是_____(选填字母代号)。
a.NaOH溶液 b.水 c.饱和NaCl溶液 d.苯乙烯
(5)实验IV时,应对量气管多次读数,读数时应注意:①将实验装置恢复到室温,②_________,③读数时,视线与凹液面最低处水平相切。经多次重复实验,获得以下数据(所有气体体积均已换算成标准状况,忽略滴入液体体积对气体体积的影响)
编号 | 某硅铁合金质量 | 量气管第一次读数 | 量气管第二次读数 |
① | 1.0g | 10.0 mL | 346.3mL |
② | 1.0g | 10.0mL | 336.0mL |
③ | 1.0g | 10.0mL | 345.7mL |
根据上述数据,可计算出硅铁合金中硅的质量分数为____。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省高三下学期3月月考理综化学试卷(解析版) 题型:选择题
化学方程式可简明地体现元素及其化合物的性质。已知:
氧化还原反应:2FeCl3+2HI=2FeCl2+I2+2HCl;2Co(OH)3+6HCl =2CoCl2+Cl2↑+6H2O;
2Fe(OH)2+ I2+2KOH = 2Fe(OH)3+2KI; 3I2+6KOH=5KI+KIO3+3H2O
复分解反应:2HSCN +K2CO3 = 2KSCN + CO2 ↑ + H2O; KCN + CO2 + H2O = HCN + KHCO3
热分解反应:4NaClO 3NaCl + NaClO4;NaClO4
3NaCl + NaClO4;NaClO4  NaCl + 2O2↑
NaCl + 2O2↑
下列说法不正确是
A.酸性(水溶液):HSCN > H2CO3 > HCN
B.还原性(碱性溶液):Fe(OH)2 > I2 > KIO3
C.热稳定性:NaCl > NaClO4 > NaClO
D.氧化性(酸性溶液):FeCl3 > Co(OH)3 > I2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省长望浏宁四县高三一模考试化学试卷(解析版) 题型:填空题
【化学-选修3物质结构与性质】(15分)早期发现的一种天然二十面体准晶颗粒由Al、Cu、Fe三种金属元素组成。回答下列问题:
(1)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过________方法区别晶体、准晶体和非晶体。
(2)基态Fe原子有_______个未成对电子,Fe3+的电子排布式为_________。可用硫氰化钾检验Fe3+,形成的配合物的颜色为____________。
(3)新制的Cu(OH)2可将乙醛(CH3CHO)氧化成乙酸,而自身还原成Cu2O。乙醛中碳原子的杂化轨道为___________,1mol乙醛分子中含有的 键的数目为___________。乙酸的沸点明显高于乙醛,其主要原因是___________ 。Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和定点,则该晶胞中有 个铜原子。
键的数目为___________。乙酸的沸点明显高于乙醛,其主要原因是___________ 。Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和定点,则该晶胞中有 个铜原子。
(4)Al单质为面心立方晶体,其晶胞参数 nm,晶胞中铝原子的配位数为 。列式表示Al单质的密度 g
nm,晶胞中铝原子的配位数为 。列式表示Al单质的密度 g cm-3。
cm-3。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省长望浏宁四县高三一模考试化学试卷(解析版) 题型:选择题
Q、W、X、Y、Z是原子序数依次增大的短周期元素,X的焰色反应呈黄色。Q元素的原子最外层电子数是其内层电子数的2倍。W、Z最外层电子数相同,Z的核电荷数是W的2倍。元素Y的合金是日常生活中使用最广泛的金属材料之一,下列说法正确的是
A.原子半径的大小顺序:rY> rX >rQ>rW
B.X、Y的最高价氧化物的水化物之间不能发生反应
C.Z元素的氢化物稳定性大于W元素的氢化物稳定性
D.元素Q和Z能形成QZ2型的共价化合物
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省七市教科研协作体高三3月联考化学试卷(解析版) 题型:实验题
Na2S2O3可用作照相的定影剂等。已知Na2S2O3的某些性质如下:
(Ⅰ)S2O32-能被I2氧化为S4O62-;
(Ⅱ)酸性条件下S2O32-迅速分解为S和SO2;
(Ⅲ)向Na2S2O3和Na2S混合溶液中通入SO2可制得Na2S2O3;所得产品中常含有少量Na2SO3和Na2SO4。
实验室可用如下装置(略去部分夹持仪器)模仿生成过程。

实验步骤:
(1)仪器组装完成后, ,则整个装置气密性良好。装置D的作用是 ,装置E中溶液的作用是 。
(2)先向C中烧瓶加入Na2S2O3和Na2S混合溶液,再向A中烧瓶滴加浓H2SO4。
(3)等Na2S2O3和Na2S完全消耗后,结束反应。过滤C中混合物,将溶液蒸发、结晶、过滤、洗涤、干燥,得到产品。
(4)为验证产品中含有硫酸盐,该小组设计了以下实验方案,请将方案补充完整。
实验步骤 | 预期现象或结论 |
步骤1:取少量固体样品溶于无氧蒸馏水中 | 固体完全溶解得无色澄清溶液 |
步骤2:加入过量盐酸 | |
步骤3:静置后取上清液,加入BaCl2溶液 |
(5)利用KMnO4标准溶液可以定量测定硫代硫酸钠试剂的纯度,步骤为:
①溶液配制:称取1.0g Na2S2O3试样,用新煮沸并冷却的蒸馏水溶解,最终定容至100mL。
②滴定:取10.00mL0.01mol·L-1 KMnO4标准溶液,加硫酸酸化,再加过量KI溶液。写出该反应的离子反应:
③往步骤②所得溶液加入某指示剂,用Na2S2O3滴定至终点(2S2O32- +I2 S4O62- +2I-),记录Na2S2O3溶液用量,滴定3次。指示剂最好选用 ,本次滴定时所用的玻璃仪器除锥形瓶外,还有 。
S4O62- +2I-),记录Na2S2O3溶液用量,滴定3次。指示剂最好选用 ,本次滴定时所用的玻璃仪器除锥形瓶外,还有 。
④若3次滴定Na2S2O3溶液的平均用量为12.00mL,则样品的纯度为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省七市教科研协作体高三3月联考化学试卷(解析版) 题型:选择题
化学来源于生活,也服务于生活,下列有关生活中的化学叙述正确的是
A.冰箱中使用的含氟制冷剂泄露后,会增加空气中的PM2.5
B.浓硫酸具有强腐蚀性,可用浓硫酸刻蚀石英制艺术品
C.施肥时,农家肥草木灰(有效成分K2CO3)不能与氮肥NH4Cl混合使用
D.氯气和活性炭均可作为漂白剂,若同时使用,漂白效果会明显加强
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省绥化市高三下学期开学联考化学试卷(解析版) 题型:选择题
在下列反应中,水仅作还原剂的是
A.Na2O+H2O=2NaOH B.2F2+2H2O=4HF+O2
C.Cl2+H2O=HCl+HClO D.2K+2H2O=2KOH+H2↑
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省资阳市高一上学期学期期末化学试卷(解析版) 题型:选择题
在含有Fe3+、Fe2+、Al3+、Cl-的稀溶液中,加入足量的Na2O2固体,充分反应后再加入过量的稀盐酸,溶液中离子数目变化最小的是
A.Al3+ 、Cl- B.Al3+ C.Fe2+、Cl- D.Fe3+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com