
【题目】丙烯是一种重要的有机化工原料,用于制丙烯腈、环氧丙烷、丙酮等。回答下列问题:
(1)已知:
I.C3H8(g)![]() C3H6(g)+H2(g) △H1=+124kJ/mol
C3H6(g)+H2(g) △H1=+124kJ/mol
II.2H2(g)+O2(g)=2H2O(g) △H2=-484kJ/mol
则丙烷氧化脱氢制丙烯反应2C3H8(g)+O2(g)![]() 2C3H6(g)+2H2O(g)的△H为_________kJ/mol。
2C3H6(g)+2H2O(g)的△H为_________kJ/mol。
(2)我国学者结合实验与计算机模拟结果,研究了丙烷在六方氮化硼催化剂表面氧化脱氢制丙烯的反应历程如图所示,其中吸附在催化剂表面的物种用*标注。
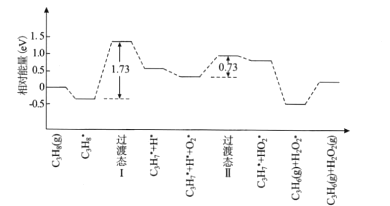
①该反应历程中决速步骤的能垒(活化能)为_________eV,该步骤的化学方程式为________
②请补充该历程之后可能发生的化学反应方程式_____________
(3)已知丙烷氧化脱氢容易发生副反应:2C3H8(g)+O2(g)![]() 3C2H4(g)+2H2O(g)如图所示是丙烷氧化脱氢制丙烯反应达到平衡时丙烷转化率与丙烯选择性随温度变化的曲线[丙烯的选择性=n=
3C2H4(g)+2H2O(g)如图所示是丙烷氧化脱氢制丙烯反应达到平衡时丙烷转化率与丙烯选择性随温度变化的曲线[丙烯的选择性=n=![]() ×100%]
×100%]
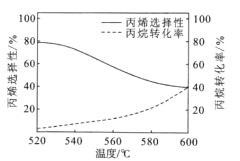
①丙烯的选择性随着温度的升高而降低的可能原因有_________
②在反应温度为600℃,将C3H8与O2以体积比为1:1充入刚性容器中,达到平衡时,丙烷的转化率为40%,丙烯的选择性也为40%,体系总压强为pkPa,则氧气的转化率![]() (O2)=______________丙烯的分压p(C3H8)=____________(结果保留2位有效数字)。
(O2)=______________丙烯的分压p(C3H8)=____________(结果保留2位有效数字)。
【答案】-236 1.73 C3H8=C3H7+H 2H2O2=2H2O+O2↑ 升高温度,催化剂的活性降低,生成丙烯的反应平衡逆向移动,生成乙烯的副反应产物参加 20% 0.087pkPa
【解析】
(1) 根据盖斯定律计算反应热;
(2)①该反应历程中决速的步骤为慢反应,活化能越大,反应速率越慢;根据活化能确定该步骤的化学方程式;
②该历程产物为双氧水,不稳定易分解,之后可能发生双氧水分解;
(3)①反应2C3H8(g)+O2(g)![]() 2C3H6(g)+2H2O(g)为吸热反应,温度过高催化剂活性降低;
2C3H6(g)+2H2O(g)为吸热反应,温度过高催化剂活性降低;
②根据图示,结合“三段式”计算。
(1)已知:I.C3H8(g)![]() C3H6(g)+H2(g) △H1=+124kJ/mol
C3H6(g)+H2(g) △H1=+124kJ/mol
II.2H2(g)+O2(g)=2H2O(g) △H2=-484kJ/mol
根据盖斯定律,I×2+ II可得:2C3H8(g)+O2(g)![]() 2C3H6(g)+2H2O(g) △H=-236kJ/mol;
2C3H6(g)+2H2O(g) △H=-236kJ/mol;
(2)①该反应历程中决速的步骤为慢反应,活化能越大,反应速率越慢,根据图示,活化能最大的为过渡态I,能垒(活化能)为1.73 eV;根据活化能确定该步骤的化学方程式为C3H8=C3H7+H;
②该历程产物为双氧水,不稳定易分解,之后可能发生双氧水分解,反应为:2H2O2=2H2O+O2↑;
(3)①反应2C3H8(g)+O2(g)![]() 2C3H6(g)+2H2O(g)为吸热反应,温度过高催化剂活性降低,则升高温度,催化剂的活性降低,生成丙烯的反应平衡逆向移动,生成乙烯的副反应产物参加;
2C3H6(g)+2H2O(g)为吸热反应,温度过高催化剂活性降低,则升高温度,催化剂的活性降低,生成丙烯的反应平衡逆向移动,生成乙烯的副反应产物参加;
②根据图示在反应温度为600℃,将C3H8与O2以体积比为1:1充入刚性容器中,达到平衡时,丙烷的转化率为40%,丙烯的选择性也为40%,体系总压强为pkPa,相同条件下,物质的量之比等于体积之比,2C3H8(g)+O2(g)![]() 2C3H6(g)+2H2O(g)和2C3H8(g)+O2(g)
2C3H6(g)+2H2O(g)和2C3H8(g)+O2(g)![]() 3C2H4(g)+2H2O(g),反应中C3H8与O2的反应比例关系相同,设C3H8与O2的起始物质的量为1mol,则:
3C2H4(g)+2H2O(g),反应中C3H8与O2的反应比例关系相同,设C3H8与O2的起始物质的量为1mol,则:
![]()
则氧气的转化率![]() (O2)=
(O2)=![]() ×100%=20%;
×100%=20%;
设平衡时,反应生成C3H6的物质的量为x,生成C2H4的物质的量为y,
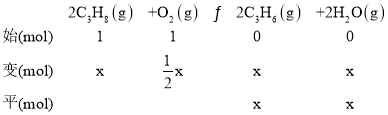
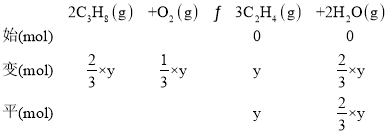
根据题意可得: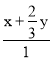 ×100%=40%,
×100%=40%,![]() 40%,解得:x=0.2mol,y=0.3mol,平衡时n(C3H8)=1mol×(1-40%)=0.6mol,n(O2)=1mol×(1-20%)=0.8mol,n(H2O)=0.2mol+
40%,解得:x=0.2mol,y=0.3mol,平衡时n(C3H8)=1mol×(1-40%)=0.6mol,n(O2)=1mol×(1-20%)=0.8mol,n(H2O)=0.2mol+![]() ×0.3mol=0.4mol,丙烯的分压p(C3H8)= pkPa×
×0.3mol=0.4mol,丙烯的分压p(C3H8)= pkPa×![]() =0.087pkPa。
=0.087pkPa。


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
【题目】在不同条件下,分别测得反应2SO2(g)+O2(g)![]() 2SO3(g)的化学反应速率,其中表示该反应进行得最快的是( )
2SO3(g)的化学反应速率,其中表示该反应进行得最快的是( )
A. υ(SO2)=4 mol·L-1·min-1B. υ(O2)=3 mol·L-1·min-1
C. υ(SO2)=0.1 mol·L-1·s-1D. υ(O2)=0.1 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四氯化锡常温下呈液态,熔点-33℃,沸点144℃,在潮湿的空气中能强烈水解生成金属氧化物并产生有刺激性的白色烟雾,可用作媒染剂、催化剂等。实验室利用如图所示装置制备四氯化锡(夹持装置略)。
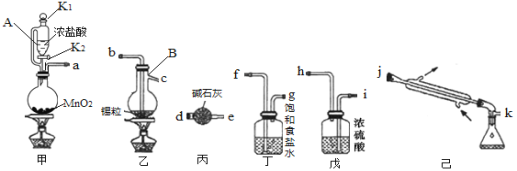
回答下列问题:
(1)甲装置中发生反应的离子方程式为_________,仪器B的名称是_____。
(2)按照气流方向连接装置,接口顺序为_________。
(3)实验开始时需向圆底烧瓶中缓慢滴加浓盐酸,此时应打开仪器A的活塞_____(填“K1”、“K2”或“K1和K2”)。排尽装置中的空气后才能点燃乙处的酒精灯,判断装置中空气已排尽的现象是______。实验结束时,应先停止加热的装置是_____(填“甲”或“乙”)。
(4)丙装置的作用是_____,若没有丙装置,可能发生的化学反应方程式为____。
(5)实验制得30g溶有氯气的SnCl4,其中氯气质量分数为13.0%,则至少需向乙中通入标准状况的氯气_______L (保留2位小数) 。提纯该SnCl4的方法是______(填序号)。
a.用NaOH溶液洗涤再蒸馏 b.升华 c.重结晶 d.蒸馏 e.过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常用小轿车(燃油汽车)中的动力和能量与化学反应息息相关。
(1)用C8H18代表汽油分子,写出汽油完全燃烧的化学方程式_____。
(2)关于汽油在气缸中燃烧反应的叙述正确的是_____
A.汽油具有的总能量高于生成物二氧化碳和水具有的总能量
B.汽油燃烧过程中,化学能转化为热能
C.断裂汽油和氧气分子中化学键吸收的能量小于生成碳氧化物和水中化学键放出的能量
D.汽车尾气中含NO的原因是汽油中含有氮元素,燃烧后生成NO
(3)汽车中的电瓶为铅酸电池,Pb+PbO2 +2H2SO4![]() PbSO4+2H2O,已知PbSO4难溶于水,下列说法正确的是_____
PbSO4+2H2O,已知PbSO4难溶于水,下列说法正确的是_____
A. 放电时,负极的电极反应式为:Pb-2e-=Pb2+
B.放电时,正极得电子的物质是PbO2
C.放电时,理论上每消耗20.7g铅,外电路中转移的电子为0.4mol
D.充电是使放电时的氧化还原反应逆向进行
(4)研究氢氧燃料电池中,H2所在的电极为_____极(填“正”或“负”),电极反应式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在室温下,向25 mL 0.1 mol/L NaOH溶液中逐滴加入0.2mol/L CH3COOH溶液,曲线如图所示。下列说法中正确的是
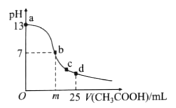
A.在b点的溶液中:m>12.5,且有c(Na+)=c(CH3COO-)=c(OH-)=c(H+)
B.在c点的溶液中:c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
C.在d点的溶液中:c(CH3COO-)+c(CH3COOH)=2c(Na+)
D.在a一b的溶液中一定都有:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关。下列说法中正确的是( )
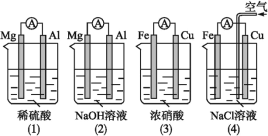
A.(1)(2)中Mg作负极,(3)(4)中Fe作负极B.(2)中Mg作正极,电极反应式为6H2O+6e-=6OH-+3H2↑
C.(3)中Fe作负极,电极反应式为Fe-2e-=Fe2+D.(4)中Cu作正极,电极反应式为2H++2e-=H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组用0.50 mol·L-1 NaOH溶液和0.50 mol·L-1 H2SO4溶液进行中和热的测定。
Ⅰ.配制0.50 mol·L-1 H2SO4溶液
(1)若配制250 mL H2SO4溶液,则需量筒量取密度为1.84 g·cm-3,质量分数为98%的浓硫酸____mL。
Ⅱ.测定稀硫酸和稀氢氧化钠反应的中和热的实验装置如图所示:
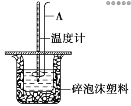
(2)仪器A的名称为___________。
(3)写出表示该反应中和热的热化学方程式:__________________。
(4)取50 mL NaOH溶液和30 mL H2SO4溶液进行实验,实验数据如下表。
实验 次数 | 起始温度t1/℃ | 终止温度t2/℃ | 温度差(t2-t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.6 | 26.6 | 26.6 | 29.1 | |
2 | 27.0 | 27.4 | 27.2 | 31.2 | |
3 | 25.9 | 25.9 | 25.9 | 29.8 | |
4 | 26.4 | 26.2 | 26.3 | 30.4 | |
①温度差的平均值为____
②近似认为0.50 mol·L-1 NaOH溶液和0.50 mol·L-1 H2SO4溶液的密度都是1 g·cm-3,中和后生成溶液的比热容c=4.18 J·(g·℃)-1。则测得的中和热ΔH=___________(取小数点后一位)。
③上述结果与57.3 kJ·mol-1有偏差,产生此偏差的原因可能是____(填字母)。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.一次性把NaOH溶液倒入盛有H2SO4溶液的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
(5)碎泡沫塑料的作用是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用价层电子对互斥理论预测H2O和BF3的立体结构,两个结论都正确的是( )
A. 直线形;三角锥形 B. V形;三角锥形
C. 直线形;平面三角形 D. V形;平面正三角形
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某可逆反应mA(g)+nB(g)pC(g)在密闭容器中进行,如图表示反应时间 t时、温度 T 和压强P 与反应混合气体中 C 的体积分数(C%)的关系曲线,由曲线分析,下列判断正确的是
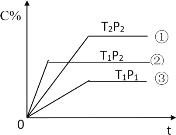
A.T1<T2 P1>P2 m+n<p ΔH>0
B.T1>T2 P1<P2 m+n>p ΔH<0
C.T1<T2 P1>P2 m+n<p ΔH<0
D.T1>T2 P1<P2 m+n>p ΔH>0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com