
【题目】25℃时,10mL 0.15mol/L的硫酸与10mL 0.1mol/L的氢氧化钠溶液混合,则混合后的pH为
A. 0 B. 1 C. 2 D. 3
科目:高中化学 来源: 题型:
【题目】工业上制备硫酸常用接触法,工业上制硝酸常用氨的催化氧化法。下列关于工业上制硫酸与硝酸的说法中不正确的是( )
A. 在沸腾炉中进行的反应为:4FeS2+11O2![]() 2Fe2O3+8SO2
2Fe2O3+8SO2
B. 制硫酸在吸收塔中是用水来吸收SO3
C. 氨催化氧化制硝酸过程中的三个主要反应都属于氧化还原反应
D. 硫酸工业、硝酸工业都需要对工业尾气进行处理
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国是干电池的生产和消费大国。某科研团队设计了以下流程对碱性锌锰干电池的废旧资源进行回收利用:

已知:①Ksp(MnS)=2.5×10-13,Ksp(ZnS)=1.6×10-24
②Mn(OH)2开始沉淀时pH为8.3,完全沉淀的pH为9.8
⑴碱性锌锰干电池是以锌粉为负极,二氧化锰为正极,氢氧化钾溶液为电解质。电池总反应为2MnO2+ Zn+2KOH= 2MnOOH+K2ZnO2,请写出电池的正极反应式_____________;
⑵为了提高碳包的浸出效率,可以采取的措施有________________________;(写一条即可)
⑶向滤液1中加入MnS的目的是__________________________________________;
⑷已知MnSO4的溶解度曲线如图所示,从滤液2中析出MnSO4·H2O晶体的操作是蒸发结晶、____________________、洗涤、低温干燥;

⑸为了选择试剂X,在相同条件下,分别用3 g碳包进行制备MnSO4的实验,得到数据如表1,请写出最佳试剂X与碳包中的主要成分发生反应的化学方程式_____________。
⑹工业上经常采用向滤液2中加入NaHCO3溶液来制备MnCO3,不选择Na2CO3溶液的原因是___________________________________;
⑺该科研小组利用EDTA(乙二胺四乙酸二钠,阴离子简写为Y2-)进行络合滴定测定Mn2+在电池中的百分含量,化学方程式可以表示为Mn2++Y2-=MnY。实验过程如下:
准确称量一节电池的质量平均为24.00g,完全反应后,得到200.00mL滤液2,量取10.00mL滤液2稀释至100.00mL,取20.00mL溶液用0.0500molL-1EDTA标准溶液滴定,平均消耗标准溶液22.00mL,则该方案测得Mn元素的百分含量为________。(保留3位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学在能源开发与利用中起到十分关键的作用。甲烷是一种新型的绿色能源,又是一种重要的化工原料。甲烷燃料电池能量转化率高,具有广阔的发展前景,现用甲烷燃料电池进行如图实验(图中所用电极均为惰性电极)

(1)电极b为______________极,溶液中OH-移向_____________极(填a或b);
(2)电极a处所发生的电极反应方程式为 ;
(3)乙装置所发生的总反应方程式 ;
(4)如图装置中盛有100mL0.2molL-1AgNO3溶液,当氢氧燃料电池中消耗氧气56mL(标准状况下)时,则此时右图装置中溶液的pH=__________(溶液体积变化忽略不计),d极增重 g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下向10mLpH=3的醋酸溶液中加入水稀释后,下列说法正确是的
A.溶液中导电粒子的数目减少
B.溶液中![]() 不变
不变
C.醋酸的电离程度增大,c(H+)亦增大
D.再加入10mLpH=11的NaOH溶液,混合液的pH=7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(15分)为研究铜与浓硫酸的反应,某化学兴趣小组进行如下实验。
实验I:反应产物的定性探究,按如图装置(固定装置已略去)进行实验:
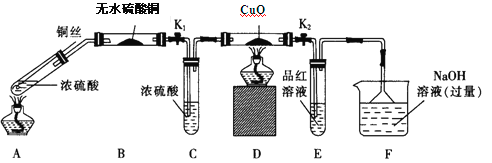
(1)F装置的烧杯中发生反应的离子方程式是 ;B装置中的现象是 。
(2)实验过程中,能证明浓硫酸中硫元素的氧化性强于氢元素的现象是 。
(3)实验结束时,撤去所有酒精灯之前必须完成的实验操作是 。
(4)实验结束后,证明A装置试管中反应所得产物是否含有铜离子的操作方法是 。
实验Ⅱ:反应产物的定量探究
(5)在铜与浓硫酸反应的过程中,发现有黑色物质出现,且黑色物质为Cu2S。产生Cu2S的反应为aCu+![]()
(6)为测定硫酸铜的产率,将该反应所得溶液中和后配制成250.00 mL溶液,取该溶液25.00 mL加入足量 KI溶液中振荡,以淀粉溶液为指示剂,用O.36 mol·![]() 的Na2S2O3溶液滴定生成的I2,3次实验平均消耗该Na2S2O3溶液25.00 mL。若反应消耗铜的质量为6.4 g,则硫酸铜的产率为 。
的Na2S2O3溶液滴定生成的I2,3次实验平均消耗该Na2S2O3溶液25.00 mL。若反应消耗铜的质量为6.4 g,则硫酸铜的产率为 。
(已知![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素X、Y、Z为前四周期元素,X的基态原子核外电子有21种运动状态,元素Y的原子最外层电子数是其内层的3倍,Z与X、Y不在同一周期,且Z原子核外p电子比s电子多5个。
⑴X基态原子的核外电子排布式为___________。
⑵X是石油化工中重要的催化剂之一,如催化异丙苯(![]() )裂化生成苯和丙烯。
)裂化生成苯和丙烯。
①1 mol苯分子中含有σ键的数目为_____________mol。
②异丙苯分子中碳原子轨道的杂化类型为_____________。
⑶与Y3分子互为等电子体的阳离子为_____________。
⑷XZ3易溶于水,熔点为960℃,熔融状态下能够导电,据此可判断XZ3晶体属于
_____________(填晶体类型)。
⑸元素Ce与X同族,其与Y形成的化合物晶体的晶胞结构如下图,该化合物的化学式为_____________。
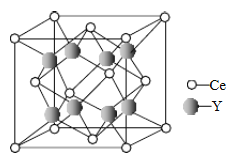
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是
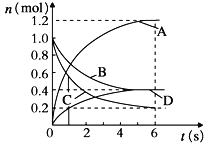
A.该反应的化学方程式为3B+4D![]() 6A+2C
6A+2C
B.反应进行到1 s时,v(A)=v(D)
C.反应进行到6 s时,B的平均反应速率为0.05 mol/(L·s)
D.反应进行到6 s时,各物质的反应速率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应C(s)+H2O(g)![]() CO(g)+H2(g)在一体积可变的密闭容器中进行。改变下列条件能增大化学反应速率的是( )
CO(g)+H2(g)在一体积可变的密闭容器中进行。改变下列条件能增大化学反应速率的是( )
①增大C(s)的用量 ②将容器的体积缩小一半 ③保持体积不变,充入N2使容器内压强增大 ④保持压强不变,充入N2使容器体积增大 ⑤保持体积不变,充入水蒸气 ⑥升高温度
A. ②⑤⑥ B. ①②③⑥ C. ②③⑤⑥ D. ①②④⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com