
 硫酸铜晶体,俗称蓝矾、胆矾,具有催吐,祛腐,解毒.取5.0g胆矾样品逐渐升高温度使其分解,分解过程的热重如表.回答下列问题:
硫酸铜晶体,俗称蓝矾、胆矾,具有催吐,祛腐,解毒.取5.0g胆矾样品逐渐升高温度使其分解,分解过程的热重如表.回答下列问题:| 温度范围/℃ | 固体质量/g |
| 258~680 | 3.20 |
| 680~1000 | 1.60 |
| 1000以上 | 1.44 |
分析 (1)测定蓝矾属于晶体的物理方法-射线衍射;根据SO42-中心原子含有的共价键个数与孤电子对个数之和确定其空间构型和杂化方式;根据价层电子对互斥理论确定其空间构型,价层电子对个数=σ键个数+孤电子对个数,据此分析解答;
(2)将硫酸铜晶体加热到258~680℃生成的物质A可由$\frac{5.0g}{250g/mol}$=$\frac{3.20}{M}$来解答;硫酸铜和氨水反应生成氢氧化铜蓝色沉淀,继续加氨水时,氢氧化铜和氨水继续反应生成络合物离子[Cu(NH3)4]2+而使溶液澄清;配合物中,配位体提供孤电子对,中心原子提供空轨道形成配位键,氨气中氮原子与氢原子存在极性键;
(3)根据加热反应,由$\frac{5.0g}{250g/mol}$=$\frac{1.44}{M}$解得M=74,去掉1个铜64,还剩下8,为Cu2O,铜是29号元素,原子核外有29个电子,根据构造原理书写铜原子基态核外电子排布式,最后写出Cu+的电子排布式;
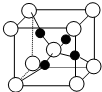
(4)①由图可知,只含有2种原子,原子个数分别8×$\frac{1}{8}$+1,4,其化学式为Cu2O,根据硫酸铜的质量计算出物质的量,再求出Cu2O的质量,由固体的质量判断温度;
②由图可知Cu的配位数为4;
③根据Cu2O晶胞结构图可知,铜原子有4个,氧原子有2个,根据ρ=$\frac{m}{V}$可计算出晶胞的体积,进而确定晶胞的边长.
解答 解:(1)X-射线衍射可用于测定蓝矾是否属于晶体;SO42-中S原子价层电子对=4+$\frac{1}{2}$(6+2-4×2)=4,且不含孤电子对,所以其立体构型是正四面体,硫原子采取sp3杂化;H2O分子中价层电子对个数=σ键个数+孤电子对个数=2+2=4,而中心原子外围只有两个原子所以含有2个孤电子对,即H2O为V型结构;
故答案为:X-射线衍射;sp3;V型;
(2)将硫酸铜晶体加热到258~680℃生成的物质A,由$\frac{5.0g}{250g/mol}$=$\frac{3.20}{M}$可得M=160g/mol,A是CuSO4;CuSO4溶于水配成溶液,加入氨水,观察到的现象是
首先形成蓝色沉淀,继续加入氨水,氢氧化铜和氨水继续反应生成络合物离子[Cu(NH3)4]2+而使溶液澄清在[Cu(NH3)4]2+离子中,Cu2+提供空轨道,NH3提供孤电子对形成配位键,N与H元素之间形成极性键;
故答案为:CuSO4;首先形成蓝色沉淀,继续加入氨水,沉淀溶解,得到深蓝色溶液;[Cu(NH3)4]2+;配位键、极性键;
(3)根据加热反应,由$\frac{5.0g}{250g/mol}$=$\frac{1.44}{M}$解得M=74,去掉1个铜64,还剩下8,为Cu2O,铜是29号元素,原子核外有29个电子,根据构造原理书写铜原子基态核外电子排布式,1s22s22p63s22p63d104s1,Cu+的电子排布式为:1s22s22p63s22p63d10;
故答案为:1s22s22p63s22p63d10;
(4)①由图可知,只含有2种原子,则为Cu和O,该晶胞中O原子数为1+8×$\frac{1}{8}$=2,Cu原子数为4,其化学式为Cu2O,硫酸铜的物质的量=$\frac{5.0g}{250g/mol}$=0.02mol,氧化亚铜的质量=0.01mol×144g/mol=1.44g,所以加热温度在1000℃以上;
故答案为:1000℃以上;
②由图可知Cu的配位数为4;
故答案为:4;
③根据Cu2O晶胞结构图可知,铜原子有4个,氧原子有2个,ρ=$\frac{m}{V}$=$\frac{\frac{144}{{N}_{A}}×2}{V}$=dg•cm-3,V=$\frac{288}{{N}_{A}•d}$,则晶胞的边长为$\root{3}{\frac{288}{{N}_{A}d}}$cm=$\root{3}{\frac{288}{{N}_{A}d}}$×1010pm,
故答案为:$\root{3}{\frac{288}{{N}_{A}d}}$×1010.
点评 本题考查较为综合,涉及配位化合物成键情况、化学键、原子杂化、空间构型、晶胞的计算等知识,题目难度中等,注意掌握均摊法在晶胞计算中的应用,试题知识点较多、综合性较强,充分考查了学生的分析、理解能力及灵活应用能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 溶液的pH增大,有O2放出 | B. | 溶质质量分数增大,有O2放出 | ||
| C. | 溶液c(Na+)增大,有O2放出 | D. | 溶液n(Na+)减小,有O2放出 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
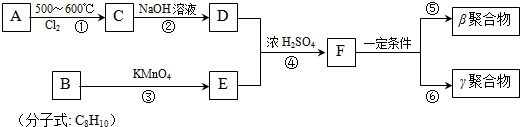
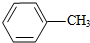 $\stackrel{MnO_{4}}{→}$
$\stackrel{MnO_{4}}{→}$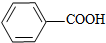
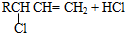 =CH2+HCl
=CH2+HCl
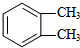 ,B苯环上的二氯代物的结构简式为:
,B苯环上的二氯代物的结构简式为: ,
, .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
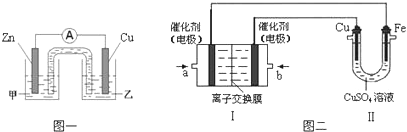
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 异戊二烯( )与等物质的量的Br2发生加成反应 )与等物质的量的Br2发生加成反应 | |
| B. | 邻羟基苯甲酸与NaHCO3溶液反应 | |
| C. | 甲苯在一定条件下发生硝化生成一硝基甲苯的反应 | |
| D. | 2一氯丁烷( )与NaOH乙醇溶液共热发生消去HCl分子的反应 )与NaOH乙醇溶液共热发生消去HCl分子的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba(OH)2与H2S04 | B. | FeBr2与Cl2 | C. | HCI与Na2CO3 | D. | NaHC03与Ca(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 它与甲醚(CH3-O-CH3)互为同分异构体 | |
| B. | 乙醇易燃烧,污染小 | |
| C. | 乙醇只能在实验室内作燃料 | |
| D. | 粮食作物是制乙醇的重要原料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com