
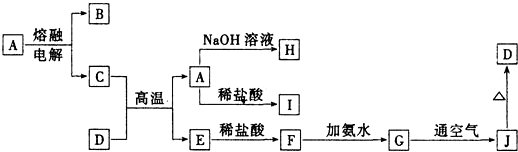
���� �������A����B��C��A��������������Һ�����ᷴӦ��A�����������ʣ�����֪A��Al2O3��H��NaAlO2��I��AlCl3��D�Ǻ���ɫ����ΪFe2O3��C��D�ķ�ӦΪ���ȷ�Ӧ����C��Al��B��O2��E��Fe��F��FeCl2��G��Fe��OH��2��J��Fe��OH��3�����������ڼ��������·ֽ��������������ݴ˽��
��� �⣺�������A����B��C��A��������������Һ�����ᷴӦ��A�����������ʣ�����֪A��Al2O3��H��NaAlO2��I��AlCl3��D�Ǻ���ɫ���壬ΪFe2O3��C��D�ķ�ӦΪ���ȷ�Ӧ����C��Al��B��O2��E��Fe��F��FeCl2��G��Fe��OH��2��J��Fe��OH��3�����������ڼ��������·ֽ�������������
��1��������������֪��AΪAl2O3������Ϊ��������H��I��Ӧ���������ﻯѧʽΪƫ�����ƺ��Ȼ���ˮ��Һ�з���˫ˮ��������������������Al3++6H2O+3AlO2-=4Al��OH��3����
�ʴ�Ϊ����������Al��OH��3��
��2��C+D��A+E�ķ�ӦΪ���ȷ�Ӧ����ѧ����ʽΪ��2Al+Fe2O3$\frac{\underline{\;����\;}}{\;}$Al2O3+2Fe��
�ʴ�Ϊ�����ȣ�
��3��G��J�Ļ�ѧ����ʽΪ��4Fe��OH��2+2H2O+O2�T4Fe��OH��3��
�ʴ�Ϊ��4Fe��OH��2+2H2O+O2�T4Fe��OH��3��
��4��C�ĵ�������һ�����õ����ȳ�����ϣ����ܽ���ǿ��NaOH��Һ��C�ĵ�����ΪAlN����NaOH��Ӧ�ķ���ʽΪAlN+NaOH+H2O=NaAlO2+NH3����
�ʴ�Ϊ��AlN+NaOH+H2O=NaAlO2+NH3����
���� ���⿼�������ƶϣ���D���ʵ���ɫ��A�ķֽ�������A��������������Һ�����ᷴӦ�����ƶ�ͻ�ƿڣ���Ҫѧ���������ն�Ԫ�ػ�����֪ʶ����Ŀ�Ѷ��еȣ�


 �����ҵ��ٿ���������������ϵ�д�
�����ҵ��ٿ���������������ϵ�д� �»����ܶ�Ա��ϵ�д�
�»����ܶ�Ա��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na | B�� | Al | C�� | Fe | D�� | Au |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
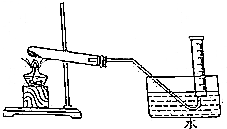 Ϊ��֤MnO2��KClO3���ȷֽ���O2�ķ�Ӧǰ���������䣬ij��ȤС��������ͼ��ʾװ�ý���������ʵ�飺
Ϊ��֤MnO2��KClO3���ȷֽ���O2�ķ�Ӧǰ���������䣬ij��ȤС��������ͼ��ʾװ�ý���������ʵ�飺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 10 mL0.1 mol•L-1��ˮ��10 mL0.1 mol•L-1�����ϣ�c��Cl-����c��NH4+����c��OH-����c��H+�� | |
| B�� | 10 mL0.1 mol•L-1NH4Cl��Һ��5 mL0.2 mol•L-1NaOH��Һ��ϣ�c��Na+��=c��Cl-����c��OH-����c��H+�� | |
| C�� | 10 mL0.1 mol•L-1CH3COOH��Һ��5 mL0.2 mol•L-1NaOH��Һ��ϣ�c��Na+��=c��CH3COO-����c��OH-����c��H+�� | |
| D�� | 10 mL0.5 mol•L-1CH3COONa��Һ��6 mL 1 mol•L-1�����ϣ�c��Cl-����c��Na+����c��OH-����c��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | +2 | B�� | +1 | C�� | 0 | D�� | -2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ʊ�Fe��OH��3���壺Fe3++3H2O$\frac{\underline{\;\;��\;\;}}{\;}$Fe��OH��3�����壩+3H+ | |
| B�� | �Ҵ��Ľṹ��ʽ��C2H6O | |
| C�� | CO2�ı���ģ�ͣ� | |
| D�� | ������Ϊ8��������Ϊ17��ԭ�ӣ�${\;}_{8}^{17}$Cl |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com