
| A.碘升华时破坏了共价键 |
| B.含极性键的共价化合物一定是电解质 |
| C.氯化钠固体中的离子键在溶于水时被破坏 |
| D.HF的分子间作用力大于HCl,故HF比HCl更稳定 |
 计算高手系列答案
计算高手系列答案科目:高中化学 来源:不详 题型:单选题
| A.13C与15N有相同的中子数 |
| B.C60与13C互为同素异形体 |
| C.15N与14N互为同位素 |
| D.15N的核外电子数与中子数相同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.键的极性N—H比P—H强 |
| B.分子的极性NH3比PH3强 |
| C.相对分子质量PH3比NH3大 |
| D.NH3分子之间存在特殊的分子间作用力 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
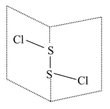
| A.S2Cl2为共价化合物 |
| B.S2Cl2只含有极性共价键 |
| C.S2Cl2与水反应时S—S键和S—Cl键都断裂 |
| D.S2Cl2分子中S—S键和S—Cl键是通过共用电子对的相互作用形成的 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
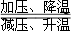 Li3BN2H8。下列有关说法正确的是
Li3BN2H8。下列有关说法正确的是| A.B的原子半径小于N的原子半径 |
| B.H2的结构式为H—H |
| C.放氢过程为化合反应 |
| D.储氢过程没有能量变化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.试管塞越来越紧,是因为反应消耗了大量O2 |
| B.打开试管塞前Cu元素的化合价为+1价 |
C.溶液迅速变为蓝色溶液,是因为反应生成了 |
| D.上述反应原理可用于测定O2的含量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.含有NH4+和H- |
| B.NH5中N元素的化合价为+5价 |
| C.1 mol NH5中含有5NA个N—H键 |
| D.与乙醇反应时,NH5被还原 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.离子晶体的晶格能越大,离子晶体的熔点越高 |
| B.碘单质在水中溶解度很小,但在CCl4中溶解度很大,这是因为CCl4和I2都是非极性分子,而H2O是极性分子 |
| C.成键原子的原子轨道重叠越多,共价键越牢固 |
| D.含有金属阳离子的晶体一定是离子晶体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.直线形 sp杂化 | B.三角形 sp2杂化 |
| C.三角锥形 sp2杂化 | D.三角锥形 sp3杂化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com