
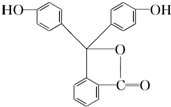
 酚酞是中学化学中常用的酸碱指示剂,其结构如下,完成下列问题:
酚酞是中学化学中常用的酸碱指示剂,其结构如下,完成下列问题: 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
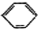
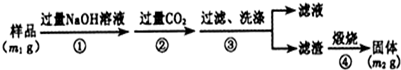
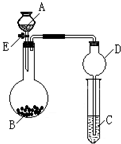 某同学设计了如图所示装置(夹持仪器省略)进行系列实验,实验时将药品A逐滴加入到固体B中,请根据下列实验回答问题:
某同学设计了如图所示装置(夹持仪器省略)进行系列实验,实验时将药品A逐滴加入到固体B中,请根据下列实验回答问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
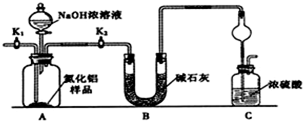
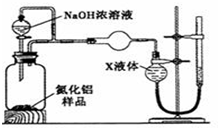
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2→MgO | B. | Fe3O4→H2O | C. | FeCl3→CuCl2 | D. | MnO2→Al2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | MnO2与浓HCl作用:MnO2+4HCl(浓)$\stackrel{△}{→}$MnCl2+Cl2↑+2H2O | |
| B. | KMnO4+16HCl(浓)→2KCl+2MnCl2↑+5Cl2↑+8H2O | |
| C. | KClO3+6HCl(浓)→KCl+3Cl2↑+3H2O | |
| D. | Ca(ClO)2+4HCl(浓)→CaCl2+2Cl2↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe-Zn合金 | B. | Fe-Cu合金 | C. | Fe-Mg合金 | D. | Mg-Al合金 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
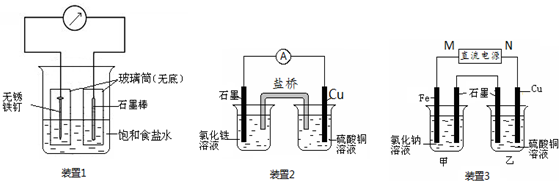
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
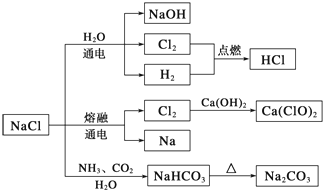
| A. | 25℃,NaHCO3在水中的溶解度比Na2CO3的大 | |
| B. | 石灰乳与Cl2的反应中,Cl2既是氧化剂,又是还原剂 | |
| C. | 电解NaCl溶液的阳极产物为H2和NaOH | |
| D. | 图中所示转化反应都是氧化还原反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com