
氮氧化合物是大气污染的重要因素。
(1)汽车排放的尾气中含NO,生成NO的反应的化学方程式为 。
(2)采取还原法,用炭粉可将氮氧化物还原。
已知: N2(g)+O2(g)=2NO(g) ΔH=+180.6 kJ·mol-1
C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
则反应 C(s)+2NO(g)=CO2(g)+N2(g) ΔH=________kJ·mol-1。
(3)将NO2变成无害的N2要找到适合的物质G与适当的反应条件,G应为 (填写“氧化剂”或“还原剂”)。下式中X必须为无污染的物质,系数n可以为0。
NO2 + G  N2 + H2O + nX(未配平的反应式)。
N2 + H2O + nX(未配平的反应式)。
下列化合物中,满足上述反应式中的G是 (填写字母)。
a.NH3 b.CO2 c.SO2 d.CH3CH2OH
(4)治理水中硝酸盐污染的方法是:
①催化反硝化法中,用H2将NO3-还原为N2,一段时间后, 溶液的碱性明显增强。则反应的离子方程式为: 。
②在酸性条件下,电化学降解NO3-的原理如下图,电源正极为: (选填“A”或“B”),阴极反应式为: 。

 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案科目:高中化学 来源:2015-2016学年广东省高二上第二次段考化学试卷(解析版) 题型:填空题
硫酸铅(PbSO4)广泛应用于制造铅蓄电池、白色颜料等。利用方铅矿精矿(PbS)直接制备硫酸铅粉末的流程如下:
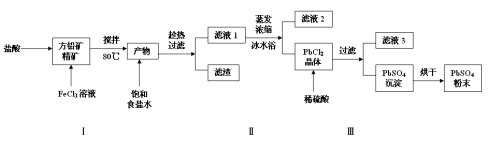
已知:(ⅰ)PbCl2(s)+2Cl-(aq) PbCl42-(aq) △H>0
PbCl42-(aq) △H>0
(ⅱ)Ksp(PbSO4)=1.08×10-8, Ksp(PbCl2)=1.6×10-5
(ⅲ)Fe3+、Pb2+以氢氧化物形式完全沉淀时,溶液的PH值分别为3.2、7.04
(1)步骤Ⅰ中生成PbCl2和S的离子方程式 ,加入盐酸的另一个目的是为了控制PH值在0.5~1.0,原因是 。
(2)用化学平衡移动的原理解释步骤Ⅱ中使用冰水浴的原因 。
(3)写出PbCl2晶体转化为PbSO4沉淀的离子方程式 。
(4)请用离子方程式解释加入H2O2后滤液2可循环利用的原因 ,滤液3是 。
(5)铅蓄电池的电解液是硫酸,充电后两个电极上沉积的PbSO4分别转化为PbO2和Pb,充电时阴极的电极反应式为 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高二上第二次段考化学试卷(解析版) 题型:选择题
用式量为43的烷基取代甲苯苯环上的一个氢原子,所得芳香烃产物的种类数为
A.3 B. 4 C.5 D.6
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高一上期中试卷化学试卷(解析版) 题型:选择题
向500mL 2mol/L 的CuSO4溶液中插入一块铁片,反应片刻后取出铁片,经洗涤、烘干,称其质量比原来增重2.0g.下列说法错误的是(设反应后溶液的体积不变)( )
A.则此过程中参加反应的铁的质量是14g
B.析出铜物质的量是0.25mol
C.反应后溶液中:c(FeSO4)=1.5mol/L
D.反应后溶液中:c(CuSO4)=1.5mol/L
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高一上期中试卷化学试卷(解析版) 题型:选择题
下列叙述不正确的是( )
A.氢氧化铁胶体带正电荷
B.胶体区别于其他分散系的本质特征是分散质的微粒直径在10﹣9﹣10﹣7m之间
C.把FeCl3饱和溶液滴入到沸腾的蒸馏水中,以制取Fe(OH)3胶体
D.Fe(OH) 3胶体的电泳实验中,阴极区颜色加深
查看答案和解析>>
科目:高中化学 来源:2016届甘肃省高三上第三次模拟考试化学试卷(解析版) 题型:选择题
关于下列各装置图的叙述中,正确的是
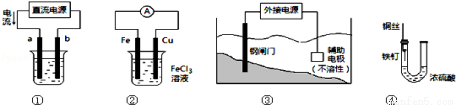
A.用装置①精炼铜,则b极为粗铜,电解质溶液为CuSO4溶液
B.装置②的总反应是:Cu+2Fe3+=Cu2++2Fe2+
C.装置③中钢闸门应与外接电源的正极相连
D.装置④中的铁钉几乎没被腐蚀
查看答案和解析>>
科目:高中化学 来源:2016届甘肃省高三上第三次模拟考试化学试卷(解析版) 题型:选择题
已知25 ℃、101 kPa下,下列反应
C(石墨) + O2(g) === CO2(g) ,燃烧1 mol C(石墨)放热393.51 kJ。
C(金刚石) + O2(g) === CO2(g),燃烧1 mol C(金刚石)放热395.41 kJ。可以得出的结论是
A.金刚石比石墨稳定 B.1 mol石墨所具有的能量比1 mol金刚石低
C.金刚石转变成石墨是物理变化 D.石墨和金刚石都是碳的同位素
查看答案和解析>>
科目:高中化学 来源:2016届甘肃省张掖市高三上第一次诊断考试理综化学试卷(解析版) 题型:选择题
NA为阿伏加德罗常数,下列叙述正确的是( )
A.1.0L1.0mo1·L-1的NaNO3水溶液中含有的氧原子数为3NA
B.0.1molCu与足量的浓硫酸反应生成SO2的体积为2.24L
C.25℃时pH=13的Ba(OH)2溶液中含有OH一的数目为0.1NA
D.反应Cl2+2NaOH=NaCl+NaClO+H2O中,每消耗1molCl2转移电子数为 NA
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一上12月月考化学试卷(解析版) 题型:选择题
下列反应中,不属于氧化还原反应的是
A.3Fe+4H2O(g)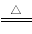 Fe3O4+4H2
Fe3O4+4H2
B.2Na+2H2O=2NaOH+H2↑
C.SnCl4+2H2O=SnO2+4HCl
D.2Na2O2+2CO2=2Na2CO3+O2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com