
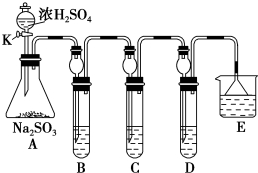
分析 (1)二氧化硫氧化性较弱,能够氧化硫化钠;
(2)高锰酸钾氧化二氧化硫生成硫酸,二氧化硫有毒,能够与氢氧化钠反应生成亚硫酸钠和水;
(3)(ⅰ)新制漂白粉浓溶液中含有的次氯酸根离子具有氧化性,能氧化亚硫酸根离子;
(ⅲ)漂白粉浓溶液中含有的次氯酸根离子具有氧化性,能氧化+4价的硫,据此书写化学方程式;
解答 解:(1)二氧化硫氧化性较弱,能够氧化硫化钠,反应得到硫单质,现象产生浑浊;
故答案为:硫化钠溶液;
(2)二氧化硫具有强的还原性,能够被酸性高锰酸钾氧化,化学方程式:5SO2+2KMnO4+2H2O=2MnSO4+K2SO4+2H2SO4;
二氧化硫有毒,能够与氢氧化钠反应生成亚硫酸钠和水,方程式:SO2+2NaOH=Na2SO3+H2O;
故答案为:5SO2+2KMnO4+2H2O=2MnSO4+K2SO4+2H2SO4;SO2+2NaOH=Na2SO3+H2O;
(3)(ⅰ)新制漂白粉浓溶液中含有的次氯酸根离子具有强氧化性,二氧化硫具有还原性,会发生氧化还原反应,生成产物为硫酸钙,
故答案为:CaSO4;
(ⅲ)漂白粉浓溶液中含有的次氯酸根离子具有氧化性,能氧化+4价的硫,所以生成该白色沉淀的化学方程式:Ca(ClO)2+H2O+SO2=CaSO4+2HCl,
故答案为:Ca(ClO)2+H2O+SO2=CaSO4+2HCl;
点评 本题主要考查了探究SO2的化学性质实验操作,掌握实验的原理及二氧化硫的性质是解题的关键,题目难度中等.


 小学期末标准试卷系列答案
小学期末标准试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 采用“绿色化学”工艺,使原料尽可能转化为所需要的物质 | |
| B. | 减少氟氯烃气体的使用,保护臭氧层免遭破坏 | |
| C. | 大量砍伐树木,制造生活必需品,从而降低物价,维持社会和谐 | |
| D. | 提倡每个人都要有“节能减排”的观念,在生活细节中也要点点滴滴地节约能源 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质的颜色随核电荷数的增加而加深 | |
| B. | 单质的熔、沸点随核电荷数的增加而升高 | |
| C. | 单质的氧化性减弱 | |
| D. | 它们的氢化物的稳定性随核电荷数的增加而增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③中加入过量的试剂是为了完全除去相应的杂质离子 | |
| B. | ③中加入过量Na2CO3溶液仅为了完全除去Ca2+ | |
| C. | 因为Mg(OH)2难溶而MgCO3微溶,所以用NaOH除Mg2+效果比用Na2CO3好 | |
| D. | ⑤中可以通过边滴加边测定溶液pH的方法,控制加入的盐酸“适量” |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质的颜色随核电荷数的增加逐渐加深 | |
| B. | 元素的最高化合价均为+7 | |
| C. | 从上到下原子半径递增 | |
| D. | 从上到下非金属性减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
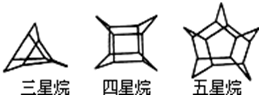
| A. | 三星烷与丙苯互为同分异构体 | B. | 五星烷的二氯取代物有8种 | ||
| C. | 六星烷的化学式为C18H24 | D. | 七星烷的一硝基取代物有2种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,5.6L四氯化碳含有的分子数为0.25NA | |
| B. | 1.4g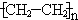 中含有的碳原子数为0.2NA 中含有的碳原子数为0.2NA | |
| C. | 1 mol苯分子中含有C=C双键数为3NA | |
| D. | 乙烷和丙烯的物质的量共1mol,完全燃烧生成水分子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两种元素 | B. | 互为同位素 | C. | 同种核素 | D. | 同一原子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com