
【题目】X、Y和Z均为短周期元素,原子序数依次增大,X的单质为密度最小的气体,Y原子最外层电子数是其周期数的三倍,Z与X原子最外层电子数相同.回答下列问题:
(1)X、Y和Z的元素符号分别为、、 .
(2)由上述元素组成的化合物中,既含有共价键又含有离子键的有、 .
(3)X和Y组成的化合物中,既含有极性共价键又含有非极性共价键的物质的电子式为此化合物在酸性条件下与高锰酸钾反应的离子方程式为;此化合物还可将碱性工业废水中的CN﹣氧化为碳酸盐和氨,相应的离子方程式为 .
【答案】
(1)H;O;Na
(2)NaOH;Na2O2
(3)![]() ;5H2O2+2MnO4﹣+6H+=2Mn2++8H2O+5O2↑;H2O2+CN﹣+OH﹣=CO32﹣+NH3↑
;5H2O2+2MnO4﹣+6H+=2Mn2++8H2O+5O2↑;H2O2+CN﹣+OH﹣=CO32﹣+NH3↑
【解析】解:X、Y和Z均为短周期元素,原子序数依次增大,X的单质为密度最小的气体,则X为H元素;Y原子最外层电子数是其周期数的三倍,最外层电子数小于或等于8(第一周期元素除外),则Y最外层电子数为6,为O元素;Z与X原子最外层电子数相同,且原子序数大于Y,所以Z为Na元素,(1)X、Y和Z的元素符号分别为H、O、Na,所以答案是:H;O;Na;(2)由H、O、Na元素组成的化合物中,既含有共价键又含有离子键的有NaOH,Na2O2 , 所以答案是:NaOH;Na2O2;(3)X和Y组成的化合物中,既含有极性共价键又含有非极性共价键的物质是过氧化氢,过氧化氢的电子式为 ![]() ,与高锰酸钾反应的离子方程式为:5H2O2+2MnO4﹣+6H+=2Mn2++8 H2O+5O2↑,过氧化氢还可将碱性工业废水中的CN﹣氧化为碳酸盐和氨,方程式为:H2O2+CN﹣+OH﹣=CO32﹣+NH3↑,所以答案是:
,与高锰酸钾反应的离子方程式为:5H2O2+2MnO4﹣+6H+=2Mn2++8 H2O+5O2↑,过氧化氢还可将碱性工业废水中的CN﹣氧化为碳酸盐和氨,方程式为:H2O2+CN﹣+OH﹣=CO32﹣+NH3↑,所以答案是: ![]() ;5H2O2+2MnO4﹣+6H+=2Mn2++8 H2O+5O2↑;H2O2+CN﹣+OH﹣=CO32﹣+NH3↑.
;5H2O2+2MnO4﹣+6H+=2Mn2++8 H2O+5O2↑;H2O2+CN﹣+OH﹣=CO32﹣+NH3↑.


科目:高中化学 来源: 题型:
【题目】表为元素周期表的一部分,其中的编号代表所对应的元素.请回答下列问题: 
(1)⑧号元素的基态原子的价电子排布式是 , 与其同周期,且基态原子的核外未成对电子数最多的元素是(写出元素符号).
(2)④号与⑦号元素形成的氧化物的熔点由高到低的是 .
(3)①号与③号元素形成的含有18电子的分子为(写出名称),该分子中③号元素的原子的杂化方式为 . ②、④、⑧三种元素的原子形成的晶体,其晶胞的结构特点如图所示,则该化合物的化学式为(用对应的元素符号表示). 
(4)下表是某些短周期元素的电负性值:
元素符号 | Li | Be | B | C | O | F | Na | Al | Si | P | S | Cl |
电负性 | 1.0 | 1.5 | 2.0 | 2.5 | 3.5 | 4.0 | 0.9 | 1.5 | 1.8 | 2.1 | 2.5 | 3.1 |
①通过分析电负性值变化规律,确定N最接近的电负性值范围:<N< .
②推测电负性值与原子半径关系是 .
③试推断:AlBr3中化学键类型是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,把试管放入盛有25度时饱和石灰水的烧杯中,试管中开始放入几小块镁片,再滴入5mL盐酸,试回答下列问题. 
(1)实验中观察到的现象是 .
(2)产生上述现象的原因是 .
(3)由此推知,MgCl2溶液和H2的总能量(填“大于”、“小于”或“等于”)镁片和盐酸的总能量.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌是一种应用广泛的金属,目前工业上主要采用“湿法”工艺冶炼锌.某含锌矿的主要成分是ZnS(还含有少量FeS等其它成分),以其为原料炼锌的工艺流程如图所示: 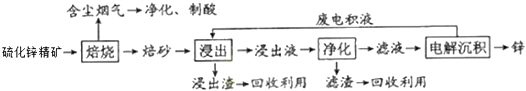
回答下列问题:
(1)硫化锌精矿的焙烧在氧气气氛的沸腾炉中进行,所产生焙砂的主要成分的化学式为 .
(2)焙烧过程中产生的含尘烟气可净化制酸,该酸可用于后续的操作.
(3)浸出液“净化”过程中加入的主要物质为 , 其作用是 .
(4)电解沉积过程中的阴极采用铝板,阳极采用Pb﹣Ag合金惰性电极,阳极逸出的气体是 .
(5)改进的锌冶炼工艺,采用了“氧压酸浸”的全湿法流程,既省略了易导致空气污染的焙烧过程,又可获得一种由工业价值的非金属单质,“氧压酸浸”中发生主要反应的离子方程式为 .
(6)我国古代曾采用“火法”工艺冶炼锌.明代宋应星著《天工开物》中有关“升炼倭铅”的记载:“炉甘石十斤,装载入一尼罐内,…,然后逐层用煤炭饼垫盛,其底铺薪,发火锻红,…,冷淀,毁罐取出,…即倭铅也.”该炼锌工艺主要反应的化学方程式为 . (注:炉甘石的主要成分为碳酸锌,倭铅是指金属锌).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.用惰性电极电解Na2SO4溶液,阴阳两极产物的物质的量之比为1:2
B.在原电池的负极和电解池的阴极上都是发生失电子的氧化反应
C.用惰性电极电解饱和NaCl溶液,若有1 mol电子转移,则生成1 molNaOH
D.镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量Fe和Fe2O3的混合物放入300mL 2mol/L的硝酸溶液中,反应完全后无固体剩余,生成4.48L NO气体(标准状况),再向反应后的溶液中加入1mol/L的NaOH溶液,要使铁元素全部沉淀下来,所加NaOH溶液的体积最少是( )
A.400mL
B.500mL
C.450mL
D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化镁是科学家们制备的一种重要化合物,它可由单只直接化合而成,它与水作用的产物之一为NH3 . 请回答下列问题:
(1)Na3N是由键形成的化合物,写出它的电子式: .
(2)Na3N与水反应属于(填基本反应类型),写出该反应的化学方程式: .
(3)Na+与N3﹣的半径关系是Na+(填“>”、“<”或“=”)N3﹣ .
(4)Mg3N2与盐酸的反应生成种盐,用电子式表示其中只含有离子键的盐的形成过程 , 写出另一种盐的电子式
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识,完成题目:
(1)在标准状况下1.7g氨气所占的体积为 , 它与同条件下molH2S含有相同的氢原子.
(2)某气体物质质量为6.4g,含有6.02×1022个分子,则该气体的摩尔质量为 .
(3)100mL、0.5mol/L的(NH4)2SO4溶液中含有NH ![]() mol,这些NH
mol,这些NH ![]() 中所含有的电子的物质的量为 , 质子的物质的量为 .
中所含有的电子的物质的量为 , 质子的物质的量为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释事实的方程式正确的是( )
A.用氯化钠溶液做导电实验,灯泡发光:NaCl ![]() Na++Cl﹣
Na++Cl﹣
B.氢氧化铁沉淀溶于氢碘酸中:Fe(OH)3+3H+═Fe3++3H2O
C.石灰水表面漂着的“白膜”可用醋酸溶解:CaCO3+2H+═Ca2++H2O+CO2↑
D.向硫酸氢钠溶液中滴加氢氧化钡溶液至刚好为中性:2H++SO42﹣+Ba2++2OH﹣═BaSO4↓+2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com