
| A. | 第15列某元素能形成碱性气体 | |
| B. | 第2列元素中肯定没有非金属元素 | |
| C. | 第17列的第一种元素的原子序数为8 | |
| D. | 短周期中能与强碱反应产生H2的金属元素位于第ⅢA族 |
分析 A.元素周期表中第15列元素为ⅤA族元素,其中N能够形成碱性气体氨气;
B.第2列元素为ⅡA元素,该族元素都是金属元素;
C.第17列元素为卤族元素,原子序数最小的为9;
D.短周期元素中能够与强碱溶液反应生成氢气的为Al.
解答 解:A.元素周期表中第15列元素为ⅤA族元素,该族元素中,N元素形成的氨气为碱性气体,故A正确;
B.第2列元素为ⅡA元素,ⅡA族元素不存在非金属元素,都是金属元素,故B正确;
C.周期表中第17列元素为ⅤⅡA族元素,又名卤族元素,该族元素中原子序数最小的为9,原子序数为8的位于ⅥA族,故C错误;
D.短周期元素中,能够与强碱溶液反应生成氢气的为金属铝,铝位于周期表中ⅢA族,故D正确;
故选C..
点评 本题考查了元素周期表和元素周期律的综合应用,题目难度中等,明确元素周期表的结构为解答关键,注意熟练掌握元素周期律内容,试题培养了学生的灵活应用能力.


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 23g Na 与足量H2O反应完全后可生成NA个H2分子 | |
| B. | 23gNO2和N2O4混合气体中含有原子总数为1.5NA | |
| C. | 足量Cu和100mL18mol/L热浓硫酸反应可生成0.9 NA个SO2分子 | |
| D. | 3mol单质Fe完全转变为Fe3O4,失去9 NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
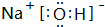 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
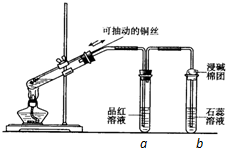 某同学设计实验证明铜与浓硫酸能发生反应,并检验生成气体的性质,如图所示,在试管里加入2mL浓硫酸,用带导管和一个小孔的胶管塞紧,从孔中插入一根铜丝,加热,把放出的气体依次通入品红溶液和石蕊溶液中.请回答下列问题:
某同学设计实验证明铜与浓硫酸能发生反应,并检验生成气体的性质,如图所示,在试管里加入2mL浓硫酸,用带导管和一个小孔的胶管塞紧,从孔中插入一根铜丝,加热,把放出的气体依次通入品红溶液和石蕊溶液中.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | I-、H+、Cl-、NO3- | B. | Al3+、K+、OH-、Ba2+ | ||
| C. | Mg2+、Fe3+、Cl-、NO3- | D. | Ca2+、SO42-、NO3-、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
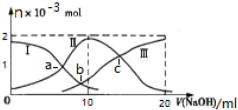 常温下,向10mL某浓度的H2SO3溶液中滴加0.2mol•L-1 NaOH溶液,含S微粒的物质的量变化曲线如图所示,下列有关说法正确的是( )
常温下,向10mL某浓度的H2SO3溶液中滴加0.2mol•L-1 NaOH溶液,含S微粒的物质的量变化曲线如图所示,下列有关说法正确的是( )| A. | 曲线Ⅱ代表H2SO3的浓度 | |
| B. | V(NaOH)=10ml时,溶液温度最高,c(H2SO3)=0.1mol•L-1 | |
| C. | 水的电离程度大小:a点<b点<c点 | |
| D. | 若c点pH=6,则K2(H2SO3)=10-8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com