
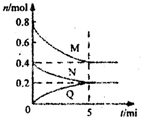
 ���ݻ�Ϊ2L�ĺ��ݵ��ܱ������У�һ���¶��£�������Ӧ��aM��g��+bN��g��?cQ��g��������M��N��Q�����ʵ�����ʱ��ı仯��ͼ��ʾ��������������ȷ���ǣ�������
���ݻ�Ϊ2L�ĺ��ݵ��ܱ������У�һ���¶��£�������Ӧ��aM��g��+bN��g��?cQ��g��������M��N��Q�����ʵ�����ʱ��ı仯��ͼ��ʾ��������������ȷ���ǣ�������A�����¶��´˷�Ӧ��ƽ�ⳣ����ֵK=
| ||
| B���÷�Ӧǰ5min��ƽ�����ʣ�v��N��=0.002mol?L-1?min-1 | ||
| C����5minʱ��������ϵ�г�������He�����´ﵽƽ��ǰv��������v���棩 | ||
| D������ʼʱ�������г���2mol M��1mol N���ﵽƽ��ʱ��M���������С��50% |
| 0.4mol |
| 2L |
| 0.2mol |
| 2L |
| c(Q) |
| c2(M)?c(N) |
| 0.1 |
| 0��22?0.1 |
| ��n(N) |
| V?��t |
| 0.2mol |
| 2L?5min |
| 0.2mol |
| 0.2mol+0.1mol+0.1mol |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������ɳ���úͨ������������Һ���ȶ���;��ʵ�����ۺ����� |
| B�������������Դ����ҵ�Ͽ��õ��ˮ������������Դ |
| C������ˮ��Ͷ���������������ɵĽ��徻ˮ��Al3++3H2O?Al��OH3�������壩+3H+ |
| D�����⻯ѧ�������������������ꡱ���γɶ��뵪���������й� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����Ħ����ʱ�þƾ�ϴ�Ӳ�Ʒ���ư�˾ƥ��ʱ����ˮϴ�Ӳ�Ʒ |
| B��������������ʱ��Ϊ�õ��ϴ�����ľ��壬Ӧ��Ȼ��ȴ�������ù�ҹ |
| C������ʳ�����Ậ���IJⶨ��ʵ��ʱ�������Ƚ�����ʳ��ϡ��10����Ȼ����ϴ������ʽ�ζ�����ȡһ�������ϡ��Һ�ڽྻ����ƿ�У���ƿ����Ҫ���ô�����Һ��ϴ |
| D��������пǰ����Ҫ��ɰֽ��ĥֱ�������ù⻬��Ȼ���������������Һ�н���5���ӣ���ˮϴ���������ϡ�����н��ݣ�����ˮϴ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��v��A��=0.3 mol/��L?min�� |
| B��v��A��=0.01 mol/��L?s�� |
| C��v��C��=0.5 mol/��L?min�� |
| D��v��B��=0.6 mol/��L?min�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ͬϵ��һ������ͬһͨʽ |
| B��ͬ���칹��һ��������ͬ�����ʽ |
| C����Է���������ȵ������л���ض���ͬ���칹�� |
| D��ͬ���칹��䲻һ�������ƵĻ�ѧ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����³�ѹ�£�8g O2����4NA������ |
| B��1L 0.1mol?L-1�İ�ˮ����NA��NH4+ |
| C�����³�ѹ�£�22.4L������������þ�۷�Ӧ��ת�Ƶĵ�����Ϊ2NA |
| D��1mol Na�ڿ�����ȼ��ʧȥ2NA������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Q3��Q2��Q1 |
| B��Q1��Q2��Q3 |
| C��Q1��Q3��Q2 |
| D��Q2��Q1��Q3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ԭ�Ӱ뾶��Z��Y��W�������Ӱ뾶��W��Y��Z |
| B��W���Ȼ���ˮ��Һ�еμӹ���Z�����γɵı�����Һ��������W����� |
| C������X��Y��Z����ε�ˮ��Һ�����ԣ�����Һ�и���������Ũ�ȴ����������Ũ�� |
| D����֪YX3�е�Զ����YZ3����Y-X���ļ��ܸ���Y-Z�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���е��С��ϵΪ�����ˮ���Ҵ��������飾��ȩ |
| B����ˮ���ܽ�ȴ�С��ϵΪ�����������������ӣ��Ҵ� |
| C����ˮ�������𱽡���ȩ�����Ȼ�̼�����ᡢ����������Һ�� |
| D����ȩ����������Ȼ�ϣ��������Ļ������ȫȼ�պ�����������CO2����ͬ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com