
尿素是第一个人工合成的有机物,下列关于尿素的叙述不正确的是 ( )。
| A.尿素是一种氮肥 |
| B.尿素是人体新陈代谢的一种产物 |
| C.尿素能发生水解反应 |
| D.尿素是一种酸性物质 |
科目:高中化学 来源: 题型:填空题
丙酸的结构为CH3—CH2—COOH,丙酸盐是安全有效的防霉、防腐剂,一种以碱式碳酸锌为原料的生产工艺流程如下:
| 序号 | n(丙酸)∶ n(碱式碳酸锌) | 反应温度/℃ | 丙酸锌产率/% |
| 1 | 1∶0.25 | 60 | 67.2 |
| 2 | 1∶0.25 | 80 | 83.5 |
| 3 | 1∶0.25 | 100 | 81.4 |
| 4 | 1∶0.31 | 60 | 89.2 |
| 5 | 1∶0.31 | 80 | 90.1 |
| 6 | 1∶0.31 | 100 | 88.8 |
 ,反应温度 ℃。
,反应温度 ℃。 查看答案和解析>>
科目:高中化学 来源: 题型:填空题
磷酸亚铁锂LiFePO4是一种新型汽车锂离子电池的电极材料。某化工厂以铁红、锂辉石LiAl(SiO3)2(含少量Ca2+、Mg2+的盐)、碳粉等原料来生产磷酸亚铁锂。其主要工艺流程如下: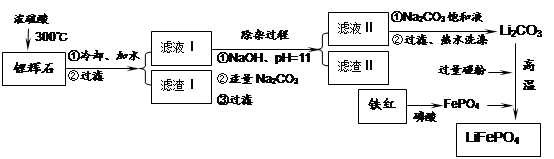
已知:2LiAl(SiO3)2 + H2SO4(浓) 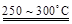 Li2SO4 + Al2O3·4SiO2·H2O↓
Li2SO4 + Al2O3·4SiO2·H2O↓
| 温度/℃ | 20 | 40 | 60 | 80 |
| 溶解度(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
| 溶解度(Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.7 |
 LiFePO4,电池中的固体电解质可传导Li+。试写出该电池放电时的正极反应: 。若用该电池电解饱和食盐水(电解池电极均为惰性电极),当电解池两极共有4480mL气体(标准状况)产生时,该电池消耗锂的质量为 。
LiFePO4,电池中的固体电解质可传导Li+。试写出该电池放电时的正极反应: 。若用该电池电解饱和食盐水(电解池电极均为惰性电极),当电解池两极共有4480mL气体(标准状况)产生时,该电池消耗锂的质量为 。查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在硫酸工业生产中,为了有利于SO2的转化,且能充分利用热能,采用了中间有热交换器接触室(见图)。按此密闭体系中气体的流向,则在A处流出的气体为( )
| A.SO2 | B.SO3、O2 | C.SO2、SO3 | D.SO2、O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列物质的工业制备原理的方程式书写正确的是
A.氢氧化钠:Na2CO3+Ca(OH)2 CaCO3↓+2NaOH CaCO3↓+2NaOH |
B.乙醇:C6H12O6 2C2H5OH+2CO2↑ 2C2H5OH+2CO2↑ |
C.二氧化硫:Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O CuSO4+SO2↑+2H2O |
D.氯气:Ca(ClO)2+4HCl(浓) CaCl2+2Cl2↑+2H2O CaCl2+2Cl2↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
如图是现今常规生产发烟硫酸和硫酸的流程图:
(1)在④处二氧化硫被氧化成三氧化硫,④的设备名称是 ,该处发生反应的方程式为 ,为提高三氧化硫的产率,该处应采用 (填“等温过程”或“绝热过程”)为宜。
(2)在⑦处进行二次催化处理的原因是 。
(3)⑤处气体混合物主要是氮气和三氧化硫.此时气体经过⑥后不立即进入⑦是因为 。
(4)20%的发烟硫酸(SO3的质量分数为20%)1吨需加水 吨(保留2位有效数字)才能配制成98%的成品硫酸。
(5)在②处发生1500℃的“不完全燃烧”,即先混入少量干燥空气,然后在③处于700℃下再继续燃烧.试简述这种燃烧方式对环境保护是有利的原因 。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列物质的制备,符合工业生产实际的是( )
| A.将氯气通入澄清石灰水中制漂白粉 |
| B.用离子交换膜法电解饱和食盐水制备烧碱、氢气和氯气 |
| C.将氢气和氯气混合后点燃,产物用水吸收制备盐酸 |
| D.将SO2和O2的混合气加高压后,通过接触室,制备SO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
(1)1791年,法国医生路布兰首先获得制碱专利,以食盐、浓硫酸、石灰石、煤为原料制碱,该方法分三步:
①用NaCl与H2SO4反应制Na2SO4;2NaCl+H2SO4 Na2SO4+2HCl↑
Na2SO4+2HCl↑
②用焦炭还原Na2SO4制Na2S;Na2SO4+4C Na2S+4CO↑
Na2S+4CO↑
③用硫化钠与石灰石反应制Na2CO3;Na2S+CaCO3 Na2CO3+CaS
Na2CO3+CaS
(2)下列说法正确的是 ( )。
| A.②③两步都是氧化还原反应 |
| B.只有第②步是氧化还原反应 |
| C.该方法对生产设备基本没有腐蚀 |
| D.该方法对环境污染较小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com