
(1)AgNO3的水溶液呈 (填“酸”、“中”、“碱”)性,实验室
在配制AgNO3溶液时, 常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的
浓度,以 (填“促进”、“抑制”)其水解。
(2)氯化铝水溶液呈 性 ,原因是(用离子方程式表示):
_________________________________; 把AlCl3溶液蒸干,灼烧,最后得到的主要固
体产物是 _______ 。
(3)在配制硫化钠溶液时,为了防止发生水解,可以加入少的 ___________________。
原因是: _______________________________________________ (用离子方程式表示) 。
 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:
【化学——选修2化学与技术】
铝生产产业链由铝土矿开采、氧化铝制取、铝的冶炼和铝材加工等环节构成。请回答下列问题:
⑴工业上采用电解氧化铝-冰晶石(Na3AlF6)熔融体的方法冶炼得到金属铝:
2Al2O3  4Al+3O2↑加入冰晶石的作用:_______________________________。
4Al+3O2↑加入冰晶石的作用:_______________________________。
⑵上述工艺所得铝材中往往含有少量Fe和Si等杂质,可用电解方法进一步提纯,该电解池中阳极的电极反应式为 ,下列可作阴极材料的是________________。
A.铝材 B.石墨 C.铅板 D.纯铝
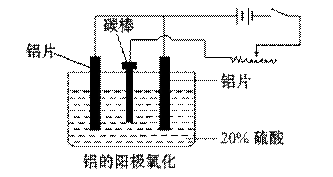
⑶阳极氧化能使金属表面生成致密的氧化膜。以稀硫酸为电解液,铝阳极发生的电极反应式为__________________________________。
⑷在铝阳极氧化过程中,需要不断地调整电压,理由是____________ 。
⑸下列说法正确的是 。
A. 阳极氧化是应用原电池原理进行金属材料表面处理的技术
B. 铝的阳极氧化可增强铝表面的绝缘性能
C. 铝的阳极氧化可提高金属铝及其合金的耐腐蚀性,但耐磨性下降
D. 铝的阳极氧化膜富有多孔性,具有很强的吸附性能,能吸附染料而呈各种颜色
查看答案和解析>>
科目:高中化学 来源: 题型:
NaH2PO4、Na2HPO4可用于合成化工原料三聚磷酸钠(Na5P3O10)。
(1)能说明NaH2PO4溶液显弱酸性原因的离子方程式为 ▲ 。
(2)能说明Na2HPO4溶液显弱碱性原因的离子方程式为 ▲ 。
(3)测定某三聚磷酸钠试样中Na5P3O10的含量可用间接滴定法,其流程如下:

①滴定时所用的指示剂X可为 ▲ 。
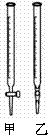
②NaOH标准溶液应盛放在右上图所示的滴定管  ▲ (选填:“甲”或“乙”) 中。
▲ (选填:“甲”或“乙”) 中。
③滴定实验记录如下表(样品中杂质不与酸或碱反应)。
| 滴定次数 | 待测溶液A的体积(/mL) | 0.1000mol·L-1NaOH溶液的体积 | |
| 滴定前读数(/mL) | 滴定后读数(/mL) | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
试计算样品中Na5P3O10的质量分数(列出计算过程,结果保留三位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列热化学方程式书写正确且对应的△H与括号内表述相符的是
A.2H2 (g) + O2 (g) = 2H2O (l) ΔH = -571.6 kJ/mol(燃烧热)
B.NaOH(aq)+ CH3COOH(aq)=CH3COONa(aq)+H2O(l);
△H=-57.3kJ/mol(中和热)
C.H2O (g) = H2 (g) + 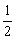 O2 (g) ΔH = -242 kJ/mol (反应热)
O2 (g) ΔH = -242 kJ/mol (反应热)
D.C(s)+ O2 ( g ) = CO2(g) ΔH =-393.5 kJ/mol(反应热)
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应2SO2(g) + O2(g)  2SO3(g) ΔH= -198kJ·mol-1,向某体积恒定的密闭容器中充入1mol SO2和0.5molO2,在一定条件下发生反应,下图是某物理量(Y)随时间(t)变化的示意图,下列说法正确的是
2SO3(g) ΔH= -198kJ·mol-1,向某体积恒定的密闭容器中充入1mol SO2和0.5molO2,在一定条件下发生反应,下图是某物理量(Y)随时间(t)变化的示意图,下列说法正确的是
A.温度T2>T1
B.反应达到平衡后放出99 kJ的热量
C.Y可能是SO2的转化率或SO3的浓度
D.反应达到平衡后容器内气体的密度减小
查看答案和解析>>
科目:高中化学 来源: 题型:
物质间纷繁复杂的转化关系是化学的魅力所在,下列选项中物质的转化在一定条件下不能实现的是( )
| 选项 | 转化关系 |
| A | Si |
| B | NO2 |
| C | Fe |
| D | S |
查看答案和解析>>
科目:高中化学 来源: 题型:
某校学生课外活动小组的同学设计下图所示实验装置,用来验证一氧化碳具有还原性。回答下列问题:

(1)装置B中最适宜的试剂的名称是 饱和碳酸氢钠溶液 ,其作用是 除去CO2中混有的HCl 。
(2)装置C的作用是 干燥CO2 ,若实验中没有装置C,则不可证明CO具有还原性,其原因是 C和H2O反应生成的H2也能还原氧化铜 。
(3)装置D中黑色固体为 C ,反应的化学方程式为 CO2+C 2CO 。
(4)根据实验中的 E中黑色固体变红 现象,可证明CO具有还原性,有关反应的化学方程式是________________________________________________________________________
________________________________________________________________________。
(5)若要根据装置F中出现的现象确认一氧化碳具有还原性,应在上图装置 D 与 E 之间连接下图中的装置 ② (填序号)。
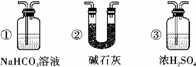
查看答案和解析>>
科目:高中化学 来源: 题型:
某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如下图所示:
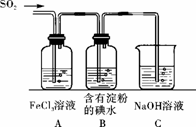
(1)SO2与FeCl3溶液反应的离子方程式为________________________________________________________________________
________________________________________________________________________。
(2)下列实验方案适用于在实验室制取所需SO2的是 BD (填序号)。
A.Na2SO3溶液与HNO3 B.Na2SO3固体与浓硫酸
C.固体硫在纯氧中燃烧 D.铜与热浓H2SO4
(3)装置C的作用是 吸收SO2尾气,防止污染空气 。
(4)若要从A中所得溶液提取晶体,必须进行的实验操作步骤:蒸发、冷却结晶、 过滤 、自然干燥,在这一系列操作中没有用到的仪器有 BF (填序号)。
A.蒸发皿 B.石棉网 C.漏斗
D.烧杯 E.玻璃棒 F.坩埚
(5)在上述装置中通入过量的SO2,为了验证A中SO2与Fe3+发生了氧化还原反应,他们取A中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液加入KMnO4溶液,紫红色褪去。
方案②:往第二份试液加入KSCN溶液,不变红,再加入新制的氯水,溶液变红。
方案③:往第三份试液加入用稀盐酸酸化的BaCl2,产生白色沉淀。
上述方案不合理的是 方案① ,原因是 A的溶液中含有SO2,SO2也能使KMnO4溶液褪色 。
(6)能表明I-的还原性弱于SO2的现象是 B中蓝色溶液褪色 。
查看答案和解析>>
科目:高中化学 来源: 题型:
将10 g铁碳合金放入O2中高温灼烧,反应后的气体通入过量石灰水中得沉淀1.4 g,则此铁碳合金是( )21cnjy.com
A.生铁 B.高碳钢
C.中碳钢 D.低碳钢
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com