
下列各组比较中,前者比后者大的是( )
|
| A. | 25℃时,pH均为2的H2SO4溶液和盐酸中氢离子的物质的量浓度 |
|
| B. | 25℃时,pH均为2的盐酸和CH3COOH溶液中溶质的物质的量浓度 |
|
| C. | 同温度、同浓度的NaCl溶液和氨水的导电能力 |
|
| D. | 25℃时,pH均为3的HCl和FeCl3溶液中水的电离程度 |
考点:
电解质在水溶液中的电离;弱电解质在水溶液中的电离平衡.
专题:
电离平衡与溶液的pH专题.
分析:
A.pH均为2,C〔H+〕=1×10﹣2mol/L;
B.盐酸是强酸完全电离,乙酸是弱酸部分电离;
C.氯化钠是强电解质完全电离,氨水是弱电解质部分电离;
D.盐酸是强电解质完全电离,三氯化铁是强酸弱碱盐水解;
解答:
解:A.根据pH=﹣lgC〔H+〕公式,pH均为2,H2SO4溶液和盐酸中氢离子的物质的量浓度C〔H+〕=1×10﹣2mol/L,两者相等,故A错误;
B.根据pH=﹣lgC〔H+〕公式,pH均为2,H2SO4溶液和盐酸中氢离子的物质的量浓度C〔H+〕=1×10﹣2mol/L,盐酸是强酸完全电离,所以,盐酸的物质的量浓度等于1×10﹣2mol/L,乙酸是弱酸部分电离,它的物质的量的浓度大于1×10﹣2mol/L,前者小,后者大,故B错误;
C.同温度、同浓度的NaCl溶液和氨水,氯化钠是强电解质完全电离NaCl=Na++Cl﹣,电离出的离子浓度等于氯化钠浓度的两倍,而氨水是弱电解质,部分电离,所以电离出的离子小于其浓度的了两倍,离子浓度大导电能力强,所以,导电能力前者比后者大,故C正确;
D.水的电离方程式:H2O⇌H++OH﹣,加入酸或碱抑制水的电离,加入能水解的盐促进水的电离,盐酸是强电解质完全电离,三氯化铁是强酸弱碱盐水解,所以前者抑制水的电离,后者促进水的电离,前者小于后者,故D错误;
故选C.
点评:
本题考查了水的电离和强弱电解质的电离,注意pH=﹣lgC〔H+〕公式与氢离子浓度间的关系,题目不难.


科目:高中化学 来源: 题型:
一些烷烃的燃烧热数值(kJ·mol﹣1)如下:
| 化合物 | 甲烷 | 乙烷 | 丙烷 | 正丁烷 | 异丁烷 | 异戊烷 |
| 燃烧热 (kJ·mol﹣1) | 891.0 | 1560.8 | 2221.5 | 2878.0 | 2869.6 | 3531.3 |
下列推断正确的是
A.正丁烷 异丁烷 △H<0
异丁烷 △H<0
B.乙烷燃烧的热化学方程式为: 2C2H6(g)+7O2(g)===CO2(g)+6H2O(g) △H=﹣1560.8 kJ·mol﹣1
C.正戊烷的燃烧热数值小于3531.3 kJ·mol﹣1
D.相同质量的烷烃,随碳原子数增加,燃烧放出的热量增多
查看答案和解析>>
科目:高中化学 来源: 题型:
关于化学反应中能量变化的说法不符合事实的是( )
|
| A. | 化学键断裂吸收能量,化学键生成放出能量 |
|
| B. | 化学反应中有物质变化也有能量变化 |
|
| C. | 需要加热的化学反应不一定是吸热反应 |
|
| D. | 图中所示的反应为放热反应
|
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物的结构为HO﹣CH2﹣CH=CHCH2﹣COOH,该有机物不可能发生的化学反应是( )
|
| A. | 水解反应 | B. | 酯化反应 | C. | 加成反应 | D. | 氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
苯是一种常见的有机溶剂和化工原料,下列关于苯的叙述正确的是( )
|
| A. | 难溶于水 | B. | 易挥发,有毒性 |
|
| C. | 属于高分子化合物 | D. | 属于烃类化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各溶液中,微粒的物质的量浓度关系正确的是( )
|
| A. | 10 mL 0.5 mol•L﹣1CH3COONa溶液与6 mL 1 mol•L﹣1盐酸混合:c(Cl﹣)>c(Na+)>c(OH﹣)>c(H+) |
|
| B. | 0.1 mol•L﹣1pH为4的NaHB溶液中:c(HB﹣)>c(H2B)>c(B2﹣) |
|
| C. | 在NaHA溶液中一定有:c(Na+)+c(H+)=c(HA﹣)+c(OH﹣)+c(A2﹣) |
|
| D. | 0.1 mol•L﹣1CH3COONa溶液中:c(OH﹣)=c(CH3COOH)+c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
在﹣50℃时,液氨的电离跟水的电离相似,存在平衡,2NH3(l)⇌N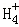 +N
+N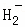 ,N
,N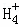 的平衡浓度为1×10﹣15mol•L﹣1,下列说法错误的是( )
的平衡浓度为1×10﹣15mol•L﹣1,下列说法错误的是( )
|
| A. | 在液氨中加入NaNH2,可使液氨的离子积变大 |
|
| B. | 在液氨中加入NH4Cl,液氨的离子积不变 |
|
| C. | 此温度下液氨的离子积K为1×10﹣30 |
|
| D. | 在液氨中加入金属钠可能有NaNH2生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
有关碰撞理论,下列说法中正确的是( )
|
| A. | 具有足够能量的分子(活化分子)相互碰撞就一定能发生化学反应 |
|
| B. | 增大反应物浓度,可增大活化分子的百分数,从而使有效碰撞次数增大 |
|
| C. | 升温能使化学反应速率增大,主要原因是增加了反应物分子中活化分子的百分数 |
|
| D. | 催化剂不影响反应活化能,从而只影响反应速率不影响化学平衡 |
查看答案和解析>>
科目:高中化学 来源: 题型:
1996年诺贝尔化学奖授予斯莫利等三位化学家,以表彰他们发现富勒烯(C60)开辟了化学研究的新领域.后来,人们又发现了一种含碳量极高的链式炔烃──棒碳,它是分子中含300~500个碳原子的新物质,其分子中只含有交替连接的单键和叁键.对于C60与棒碳,下列说法正确的是( )
|
| A. | C60与棒碳中所有的化学键都是非极性共价键 |
|
| B. | 棒碳不能使溴水褪色 |
|
| C. | C60在一定条件下可能与CuO发生置换反应 |
|
| D. | 棒碳与乙炔互为同系物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com