
| A.②④⑤ | B.①③⑥ | C.①③④ | D.②⑤⑥ |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:实验题
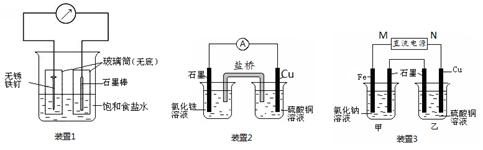
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
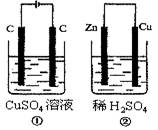
| A.右边电极上生成物质的物质的量:①=② |
| B.相同状态下电极上产生气体的体积:①=② |
| C.溶液的pH变化:①减小,②增大 |
| D.电极反应式①中阴极Cu2++2e-=Cu:②中负极:Zn-2e-=Zn2+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
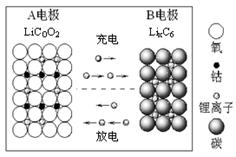
 Li1-xCoO2+LixC6
Li1-xCoO2+LixC6查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.纯镍作阳极 |
| B.阳极发生还原反应 |
| C.粗镍连接电源的正极,其电极反应为:Ni2++2e—== Ni |
| D.电解后,电解槽底部有含有Cu和Pt等金属杂质的阳极泥 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
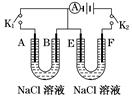

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com