
�ں��¡���ѹ�����£���ӦN2 (g)+3H2 (g) 2NH3 (g)������;���ֱ���ƽ�⣺
2NH3 (g)������;���ֱ���ƽ�⣺
��N2��H2����ʼŨ�ȷֱ�Ϊ1 mol / L��3 mol / L��
��NH3����ʼŨ��Ϊ4 mol / L�������й���������ȷ����
A��;������;�������û������İٷֺ�����ͬ
B��;����ķ�Ӧ����v (N2)��;����ķ�Ӧ����v (NH3)�ı�ֵΪ1��2
C��;��������NH3��Ũ����;��������NH3��Ũ��֮��Ϊ1��2
D��;������;��������ƽ������������ʵ���֮��Ϊ1��2
 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016��ɽ��ʡ����11���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���й���ͬ��ͬѹ�µ���������12C18O��14N2���ж���ȷ����
A��������ʱ���ܶ����  B��ԭ�������ʱ�����е����������
B��ԭ�������ʱ�����е����������
C��������ʱ�����еĵ�������� D���������ʱ�����е����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ����ѧ������ѧ��һ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪aM2����bO2��4H��===cM3����dH2O����ѧ������c��ֵΪ
A��1 B��2 C��3 D��4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ����ϳ����и߶�12���¿���ѧ���������棩 ���ͣ�ѡ����
�����е�һЩС��ʶ����������ѧ֪ʶ��������������ȷ���ǣ� ��
A����ʳ�����ůˮƿ�е�ˮ��
B����ά���������ڿ�ˮ��Ϊ�����ǣ��ʿ���Ϊ�����Ӫ������
C�����ȵĴ���ˮϴ����
D���������л������ڼ��Ի���������ɫ���ʿ����մ�ۼ���ٺ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��������������ʵ����ѧ�߶������л�ѧ���������棩 ���ͣ������
������һ�����͵���ɫ��Դ������һ����Ҫ�Ļ���ԭ�ϡ�
��1��������ȼ����ֵ�ߣ�H2(g) ��1/2 O2 (g) = H2O (g) ��H = ��241.8 kJ��mol-1
��ѧ�� | H-H | O=O | O-H |
����(kJ��mol-1) | X | 496.4 | 463 |
�����������ݼ��㣺H-H�ļ���X = ________kJ��mol-1��
��2�������ִ���ҵ����������H2��CO��Ӧ������ȼ�ϼ״����䷴Ӧ����ʽ���£�
CO2 (g) ��3H2(g) H2O(l) �� CH3OH(g) ��H = ��49.00 kJ��mol-1
H2O(l) �� CH3OH(g) ��H = ��49.00 kJ��mol-1
һ���¶��£������Ϊ1 L���ܱ������г���1.00 mol CO2��3.00 mol H2�����CO2��CH3OH��Ũ����ʱ��仯��ͼ��ʾ��
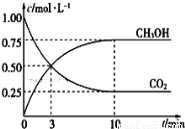
����˵���÷�Ӧ�Ѵ�ƽ��״̬����________������ţ���
A��CO2�ڻ�������е�����������ֲ���
B����λʱ����ÿ����1.2 mol H2��ͬʱ����0.4 mol H2O
C����Ӧ��H2O��CH3OH�����ʵ���Ũ�ȱ�Ϊ1��1���ұ��ֲ���
�ڴӷ�Ӧ��ʼ��ƽ��ʱ��ƽ����Ӧ����v(H2) = ________ ���ﵽƽ��ʱ������ת����Ϊ________ ��
�۸��¶��µ�ƽ�ⳣ������ʽΪ________ ��
�����е�����һ���ܼӿ췴Ӧ���ʲ������H2ת���ʵ���________������ţ���
A�����ͷ�Ӧ�¶� B�������ˮ
C����������������䣬����ϡ������ D����������������䣬����CO2����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ĵ�ʡ������ѧһ��ģ�����ۻ�ѧ�Ծ��������棩 ���ͣ������
ʯ����һ�ּ�����Ҫ����Դ���Ƿ�չ���ú���������Ҫ���ʡ�B�IJ���ͨ����������һ�����ҵ�ʯ�ͻ���ˮƽ��A�������г������л��������ˮ����������ζ��

��.�й�����ת����ϵ��ͼ1��ʾ��
��1��������Bͨ����ˮ��ʵ�������� ��
��2����Ӧ������ ��Ӧ(���л���Ӧ����)��
��3��д����Ӧ�ܵĻ�ѧ����ʽ ��
��.ij��ѧ��ȤС��Է�Ӧ�۽���̽����������ͼ2װ�ý���ʵ�飺
��4����ʵ�������θ���ܳ��������⣬��һ����Ҫ������ ��
��5����Ӧ������b�е������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���㽭��Ҧ��ѧ�߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ͼ����a ��b ������������������Һ��ζ��ĵζ����ߣ�����������ȷ����
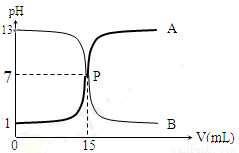
A����������ʵ���Ũ��Ϊ1 mol��L-1
B��P ��ʱǡ����ȫ�кͣ���Һ������
C������a������ζ�����������Һ�ĵζ�����
D����̪����������ʵ���ָʾ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ����ׯ���и߶�10��ѧ����黯ѧ���������棩 ���ͣ�ѡ����
��ͼΪֱ����Դ���ϡNa2SO4ˮ��Һ��װ�á�ͨ�����ʯī�缫a��b�����ֱ�μ�һ��ʯ����Һ������ʵ�������д������
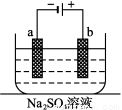
A��a�缫��������ɫ��b�缫�����ʺ�ɫ
B��a�缫�����ʺ�ɫ��b�缫��������ɫ
C���ݳ�����������a�缫�Ĵ���b�缫��
D��a��b���缫���ݳ���ɫ��ζ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��㶫ʡ�߶������в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�ݱ��������Ħ��������˾�з���һ���ɼ״��������Լ�ǿ�����������Һ�������ֻ���أ������ɴ�����ʹ�õ������ػ�﮵�ص�ʮ����������ʹ��һ���²ų�һ�ε硣���ط�ӦΪ��
2CH3OH��3O2��4OH- 2CO32-��6H2O��������˵���������
2CO32-��6H2O��������˵���������
A���ŵ�ʱCH3OH���뷴Ӧ�ĵ缫Ϊ����
B�����ʱ�������Һ��pH������
C���ŵ�ʱ�����ĵ缫��ӦʽΪ��CH3OH��6e����8OH����CO32����6H2O
D�����ʱÿ����1 mol CH3OHת��6 mol����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com