
CO2������Ҫ��������,��ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2�����ش����塣
(1)��ѧ����H2��CO2�����״�ȼ�ϡ�Ϊ̽���÷�Ӧԭ������������ʵ�飺ij�¶��£����ݻ�Ϊ2 L���ܱ������г���1 mol CO2��3.25 mol H2����һ�������·�Ӧ�����CO2��CH3OH(g)��H2O(g)�����ʵ���(n)��ʱ��ı仯��ϵ��ͼ��ʾ��
��д���÷�Ӧ�Ļ�ѧ����ʽ_______________________
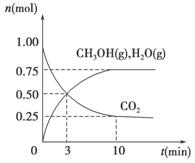 ����ӷ�Ӧ��ʼ��3 minʱ��������ƽ����Ӧ����v(H2)��____________________��
����ӷ�Ӧ��ʼ��3 minʱ��������ƽ����Ӧ����v(H2)��____________________��
�����д�ʩ��һ����ʹCO2��ת������ �����___________________ ��
�����___________________ ��
A����ԭ�������ٳ���1 mol H2 B����ԭ�������ٳ���1 mol CO2 C����С�������ݻ�
D��ʹ�ø���Ч�Ĵ��� E����ԭ�����г���1 mol He
F����ˮ��������ϵ�з����
��ѧ�һ�����������һ���������������̼��Ӧ�����Ҵ�ȼ�ϣ����Ȼ�ѧ��Ӧ����ʽΪ:2CO2(g)��6H2(g)  CH3CH2OH(g)��3H2O(g)����H��a kJ��mol��1��
CH3CH2OH(g)��3H2O(g)����H��a kJ��mol��1��
��һ��ѹǿ�£���ø÷�Ӧ��ʵ�����������ʾ������ݱ������ݻش��������⡣
|
n(H2)/n(CO2) | 500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2 | 60 | 43 | 28 | 15 |
| 3 | 83 | 62 | 37 | 22 |
��������Ӧ��a________0(����ڡ���С�ڡ�)��
�ں����£���Ӧ��ϵ�м�������������÷�Ӧ�ķ�Ӧ��aֵ________(���������С�����䡱)��
����һ���¶��£�����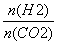 ��ֵ��CO2ת����_________�������Ҵ������ʵ���________(���������С���������䡱����ȷ����)��
��ֵ��CO2ת����_________�������Ҵ������ʵ���________(���������С���������䡱����ȷ����)��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����ж���ȷ���� �� ��
��ά����C���л�ԭ�ԣ�������������������
��NO2����ˮʱ����������ԭ��Ӧ
��1 mol Cl2�μӷ�Ӧת�Ƶ�����һ��Ϊ2NA
�������Ӷ�ֻ�л�ԭ��
��BaSO3��H2O2�ķ�ӦΪ������ԭ��Ӧ
A���٢ڢ� B���ڢۢ� C���ۢܢ� D���٢ܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪��A��B��C��D��EΪ���ڱ�1~36���е�Ԫ�أ����ǵ�ԭ������������A�Ļ�̬ԭ����3����ͬ���ܼ������ܼ��е�������ȣ�C�Ļ�̬ԭ��2p�ܼ��ϵ�δ�ɶԵ�������Aԭ����ͬ��C2—����D2�����Ӿ�����ͬ�ġ��ȶ��ĵ��Ӳ�ṹ��E�Ļ�̬ԭ�ӵ���Χ�����Ų�ʽΪ3d84s2��
��ش��������⣺
��A��B��C��D����Ԫ���У��縺�������� ����Ԫ�ط��ţ���
��B���⻯��ķе�Զ����A���⻯�����Ҫԭ���� ��
 ����A��B��C�γɵ�����CAB����AC2��Ϊ�ȵ����壬��CAB����Aԭ�ӵ��ӻ���ʽΪ ��
����A��B��C�γɵ�����CAB����AC2��Ϊ�ȵ����壬��CAB����Aԭ�ӵ��ӻ���ʽΪ ��
��E2����������AC�����γɣ�E(AC)4��2������ԭ����AC�����к��� ��
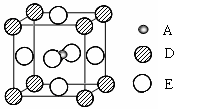
��������֣�ֻ��A��D��E����Ԫ�ص�һ�־��壨��������ͼ��ʾ�����г����ԡ�Aԭ�ӵ���λ��Ϊ ���þ���Ļ�ѧʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��B�Ļ���������ܱ������з������·�Ӧ��xA(g)+yB(g) zC(g) ��H��0��
zC(g) ��H��0��
�ﵽ��ѧƽ�����A��Ũ��Ϊ0.20 mol��L-1�������¶Ȳ��䣬���ܱ��������ݻ���С��ԭ����һ�룬�ٴδﵽƽ��ʱ�����A��Ũ��Ϊ0.35 mol��L-1���������й��ж���ȷ����
A��ƽ�����淴Ӧ�����ƶ��� B�� x+y��z
C��B��ת�����½� D��C�����������С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���б仯���������仯���� ( )
A�������ڷŵ������±�ɳ�����
B�������ڼ��������±�ɰ�ɫ��ˮ����ͭ
C��Ư�IJ�ñ���ÿ����б��
D���������������������þ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪��(1)Zn(s) + 1/2O2(g) = ZnO(s) ��H=��348.3 kJ/mol
(2)2Ag(s) + 1/2O2(g) = Ag2O(s) ��H=��31.0 kJ/mol
�� Zn(s) + Ag2O(s) = ZnO(s) + 2Ag(s) �ġ�H����( )
A��+317.3 kJ/mol B����379.3 kJ/mol
C����332.8kJ/mol D����317.3kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
(1)��MnSO4������Ļ����Һ�����K2S208(���������)����Һ�лᷢ�����·�Ӧ��Mn2++ S2082-+H2O��MnO4-+SO42һʮH+�÷�Ӧ�����ڼ���Mn2+�Ĵ��ڡ������������� ��
����Ӧ����0��1 mol��ԭ���μӷ�Ӧ�������������������ʵ���Ϊ mol��
(2)���÷�Ӧ���õ������̸�Ϊ�Ȼ��̣������������Ĺ�����ط�Ӧʱ�����и�����ء�����ء����������⣬�����������ﻹ�� ��
(3)��NaBiO3����(��ɫ��)���뵽MnSO3��H2S04�Ļ����Һ����ȣ������ܽ��Ϊ������Һ���������·�Ӧ��
NaBi03+ MnSO4+ H2S04�� Na2S04+ Bi2(S04)3+ NaMnO4+ H2O
����ƽ������Ӧ�Ļ�ѧ����ʽ��
��������Ӧ�л�ԭ������ ��
���õ����ű�ʾ��������ԭ��Ӧ
��4��S2O82-��һ�������£���ת��ΪS2O32-��д����K2S2O3�еμ�ϡ��������ӷ���ʽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
Ϊ�ᴿ��������(������Ϊ����)����ѡ�Լ�����������ȷ����
| ѡ�� | ���ʣ�������Ϊ���ʣ� | �����Լ� | ���� |
| A | �屽���壩 | CCl4 | ��Һ |
| B | ��������NO2�� | NaOH��Һ | ��Һ |
| C | ���飨��ϩ�� | ���� | ϴ�� |
| D | �Ҵ������ᣩ | NaOH��Һ | ��Һ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com