
Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如图所示,电解总反应为2Cu+H2O===Cu2O+H2↑,下列说法正确的是( )
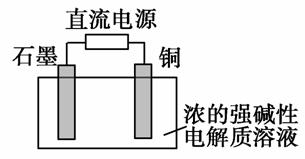
A.石墨电极上产生氢气
B.铜电极发生还原反应
C.铜电极接直流电源的负极
D.当有0.1 mol电子转移时,有0.1 mol Cu2O生成
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案科目:高中化学 来源: 题型:
在50 mL a mol·L-1的硝酸溶液中,加入6.4 g Cu,全部溶解,假设硝酸的还原产物只有NO2和NO,将反应后溶液用蒸馏水稀释至100 mL时测得c(NO )=3 mol·L-1。
)=3 mol·L-1。
(1)求稀释后的溶液c(H+)=________mol/L
(2)若a=9,则生成的气体中NO2的物质的量为________mol。
(3)治理氮氧化物污染的方法之一是用NaOH溶液进行吸收,反应原理如下:
NO2+NO+2NaOH===2NaNO2+H2O 2NO2+2NaOH===NaNO2+NaNO3+H2O
若将上述的NO2和NO的混合气体通入1 mol·L-1的NaOH恰好被吸收,NaOH溶液的体积为________mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
关于铯(Cs)及其化合物的性质,说法正确的是( )
A.金属铯的熔点比金属钠高 B.CsOH比NaOH的碱性弱
C.Cs与H2O能剧烈反应,甚至发生爆炸 D.碳酸铯难溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
某醇在适当条件下与足量的乙酸发生酯化,得到的酯的相对分子质量a与原来醇的相对分子量b的关系是a=b+84,有关该醇应该具有的结构特点的描述正确的是( )
A.该醇分子中一定具有甲基
B.该醇分子中一定没有甲基
C.该醇分子中至少含有三个碳原子
D.该醇分子中具有两个醇羟基
查看答案和解析>>
科目:高中化学 来源: 题型:
有机玻璃(PMMA)成分为聚甲基丙烯酸甲酯,因其透光性好、性能优良、价格低廉,广泛应用于商业,轻工、建筑、化工等方面,甚至人工角膜也是有机玻璃。其单体的结构和工业合成路线如图所示。
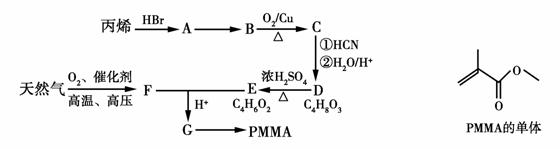
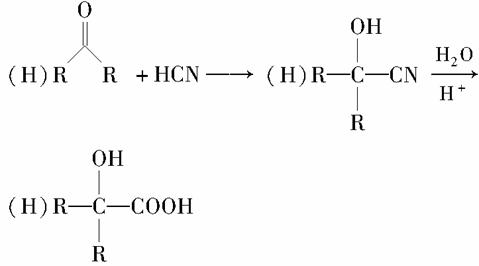
请回答下列问题:
(1)有机玻璃单体的分子式为________________。
(2)请指出反应类型:D→E属于________________反应,E+F→G属于________________反应。
(3)请指出A→B的反应条件:________________________。
(4)请写出B→C的化学方程式:______________________。
(5)写出同时符合下列条件的G的同分异构体的结构简式,请写出3种:__________________________________________________。
①能使溴水褪色;②能在碱性条件下水解;③能发生银镜反应;④具有支链。
(6)以苯乙酮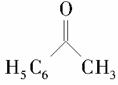 为主要原料合成
为主要原料合成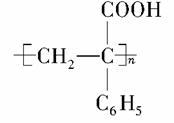 ,请设计合成路线(无机试剂任选),格式参照如下过程:CH3CHO
,请设计合成路线(无机试剂任选),格式参照如下过程:CH3CHO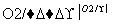 CH3COOH
CH3COOH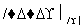 CH3COOCH2CH3。
CH3COOCH2CH3。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知一定条件下断裂或形成某些化学键的能量关系如下表:
| 断裂或形成的化学键 | 能量数据 |
| 断裂1 mol H2分子中的化学键 | 吸收能量436 kJ |
| 断裂1 mol Cl2分子中的化学键 | 吸收能量243 kJ |
| 形成1 mol HCl分子中的化学键 | 释放能量431 kJ |
对于反应:H2(g)+Cl2(g)===2HCl(g),下列说法正确的是( )
A.该反应的反应热ΔH>0
B.生成1 mol HCl时反应放热431 kJ
C.氢气分子中的化学键比氯气分子中的化学键更牢固
D.相同条件下,氢气分子具有的能量高于氯气分子具有的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
将等物质的量浓度的CuSO4溶液和NaCl溶液等体积混合后,用石墨电极进行电解,电解过程中,溶液pH随时间t变化的曲线如下图,则下列说法正确的是( )
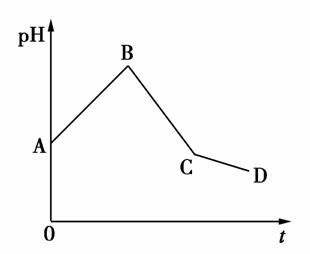
A.阳极产物一定是Cl2,阴极产物一定是Cu
B.BC段表示在阴极上是H+放电产生了H2
C.整个过程中阳极先产生Cl2,后产生O2
D.CD段表示阳极上OH-放电破坏了水的电离平衡,产生了H+
查看答案和解析>>
科目:高中化学 来源: 题型:
在一恒容的密闭容器中充入0.1 mol/L CO2、0.1 mol/L CH4,在一定条件下发生反应:CH4(g)+CO2(g)2CO(g)+2H2(g),测得CH4平衡时转化率与温度、压强关系如图,下列有关说法不正确的是( )

A.上述反应的ΔH<0
B.压强:p4>p3>p2>p1
C.1100 ℃时该反应平衡常数为1.64
D.压强为p4时,在y点:v正>v逆
查看答案和解析>>
科目:高中化学 来源: 题型:
制备氮化镁的装置示意图如下:

回答下列问题:
(1)检查装置气密性的方法是________,a的名称是________,b的名称是________。
(2)写出NaNO2和(NH4)2SO4反应制备氮气的化学方程式
________________________________________________________________________。
(3)C的作用是________,D的作用是________,是否可以把C与D的位置对调并说明理由________________________________________________________________________。
(4)写出E中发生反应的化学方程式________________________________________。
(5)请用化学方法确定是否有氮化镁生成,并检验是否含有未反应的镁,写出实验操作及现象________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com