
【题目】下列图示与对应的叙述不相符的是( ) 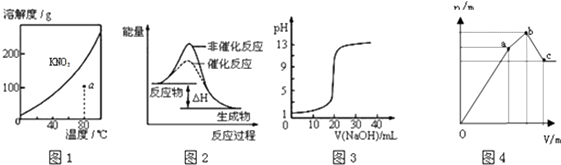
A.图1表示KNO3的溶解度曲线,图中a点所示的溶液是80℃时KNO3的不饱和溶液
B.图2表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化
C.图3表示0.1000molL﹣1NaOH溶液滴定20.00mL0.1000molL﹣1醋酸溶液得到滴定曲线
D.图4 表示向NH4Al(SO4)2溶液中逐滴滴入Ba(OH)2溶液,随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化
【答案】C
【解析】解:A、KNO3的溶解度随着温度的升高而升高,溶解度曲线上的点是饱和溶液,曲线以下的a点是不饱和溶液,故A正确;
B、反应物的总能量大于生成物的总能量,则反应是放热反应,加入催化剂会降低活化能,改变反应的速率,但反应热不改变,故B正确;
C、0.1000molL﹣1NaOH溶液滴定20.00mL 0.1000molL﹣1CH3COOH溶液,消氢氧化钠溶液体积为0时,醋酸为弱电解质,醋酸溶液的pH大于1,图象中醋酸的pH=1与实际不符,故C错误;
D、开始滴加同时发生反应为SO42﹣+Ba2+=BaSO4↓,Al3++3OH﹣=Al(OH)3↓,当Al3+沉淀完全时需加入0.03molOH﹣ , 即加入0.015molBa(OH)2 , 加入的Ba2+为0.015mol,SO42﹣未完全沉淀,此时溶液含有硫酸铵、硫酸铝;(开始到a)再滴加Ba(OH)2 , 生成BaSO4沉淀,发生反应为SO42﹣+Ba2+=BaSO4↓,NH4++OH﹣=NH3H2O,所以沉淀质量继续增加;当SO42﹣完全沉淀时,共需加入0.02molBa(OH)2 , 加入0.04molOH﹣ , Al3+反应掉0.03molOH﹣ , 生成Al(OH)30.01mol,剩余0.01molOH﹣恰好与NH4+完全反应,此时溶液中NH4+完全反应,此时溶液为氨水溶液;(a到b)继续滴加Ba(OH)2 , Al(OH)3溶解,发生反应Al(OH)3+OH﹣=AlO2﹣+2H2O,由方程式可知要使0.01molAl(OH)3完全溶解,需再加入0.005molBa(OH)2 , 此时溶液为氨水与偏铝酸钡溶液,(b到c),故D正确.
故选C.
【考点精析】通过灵活运用酸碱中和滴定,掌握中和滴定实验时,用蒸馏水洗过的滴定管先用标准液润洗后再装标准液;先用待测液润洗后在移取液体;滴定管读数时先等一二分钟后再读数;观察锥形瓶中溶液颜色的改变时,先等半分钟颜色不变后即为滴定终点即可以解答此题.


科目:高中化学 来源: 题型:
【题目】按原子序数递增的顺序(稀有气体除外),对第三周期元素性质的描述正确的是( )
A. 原子半径和离子半径均减小
B. 氧化物对应的水化物碱性减弱,酸性增强
C. 单质的晶体类型金属晶体、原子晶体和分子晶体
D. 单质的熔点降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】意大利科学家最近合成了一种新型的氧分子,其化学式为O4,对其说法正确的是( )
A. O4是一种化合物 B. O4是由O2组成的混合物
C. O4是一种单质 D. 一个O4分子由2个O2分子构成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为验证人体呼出气体中含有的CO2不是来自空气,而是人体代谢作用产生的。某学校学生课外活动小组设计了如图所示装置,你认为该装置应选用的试剂是( )

A. I是NaOH溶液 II.是Ca(OH)2溶液
B. I是Ca(OH)2溶液 II.是NaOH溶液
C. I是稀盐酸 II.是Ca(OH)2溶液
D. I是NaOH溶液 II.是CaCl2溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1)现有NaOH、Na2CO3、Ba(OH)2三种无色溶液,选用一种试剂把他们鉴别出来,并写出反应的离子方程式。
①鉴别试剂____________;
②反应的离子方程式__________________、________________、________________。
(2)某工厂的废水中含有大量的FeSO4、较多的Cu2+和少量Na+。为了减少污染并变废为宝,工厂计划从该废水中回收FeSO4和Cu。请根据流程图,在方框和括号内填写物质的名称(或主要成分的化学式)或操作方法,完成回收FeSO4和Cu的简单实验方案。_____________、_____________、_____________、_____________、_____________、_____________、_____________,
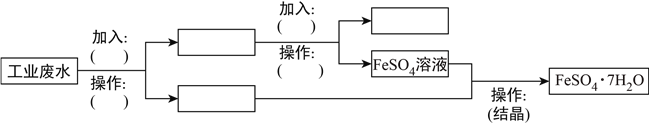
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.常温下,PH=9的碳酸钠溶液中由水电离出的c(OH﹣)=1×10﹣9molL﹣1
B.饱和氯水中:c(Cl﹣)=c(ClO﹣)+c(HClO)
C.将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低
D.中和等体积pH相同的H2SO4和HCl溶液,消耗NaOH的物质的量为2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将NH4NO3溶于水得无色溶液,为使该溶液中的c(NH ![]() ):c(NO
):c(NO ![]() )=1:1,可以采取的下列措施是( )
)=1:1,可以采取的下列措施是( )
A.加入适量的HNO3 , 抑制NH ![]() 水解
水解
B.加入适量的氨水,使溶液的pH等于7
C.再加入适量的NH4NO3(s)
D.加入适量的NaOH,使溶液的pH等于7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】制备氮化镁的装置示意图如下: 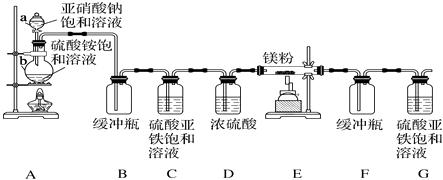
回答下列问题:
(1)仪器a的名称是 , b的名称是 .
(2)写出NaNO2和(NH4)2SO4反应制备氮气的化学方程式: .
(3)C的作用是 .
(4)写出E中发生反应的化学方程式: .
(5)请用化学方法确定氮化镁是否含有未反应的镁,写出实验操作及现象 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请填写以下空白:
(1)有以下物质: ①NaHSO4晶体 ②SO3 ③液态硫酸 ④铁 ⑤BaSO4固体 ⑥饱和 FeCl3溶液 ⑦
酒精(C2H5OH) ⑧熔融的 K2SO4,其中能导电的是__________,属于电解质的是_________,属于非电解质的是______________
(2) 化学反应 FeS+ H2SO4(浓)![]() Fe2(SO4)3+ SO2↑+ S↓+ H2O(未配平)中:
Fe2(SO4)3+ SO2↑+ S↓+ H2O(未配平)中:
氧化产物是:_______, 还原产物是:_______。
(3) 请写出醋酸与氢氧化钠溶液反应的离子方程式_______。
(4) 盐酸可以除铁锈, 请写出发生反应的离子方程式_______。
(5) 工业上常用 H2O2在酸性条件下氧化污水中的 Fe2+,请写出离子方程式:_______。
(6)某液态化合物 X2Y4常用作火箭燃料。 32 g X2Y4在一定量的 O2中恰好完全燃烧,反应方程式为: X2Y4(l)+O2(g) ![]() X2(g)+2Y2O(l)。冷却后在标准状况下测得生成物的体积为 22.4 L,其密度为 1.25 g·L-1。 X2的摩尔质量为_____________, X2Y4化学式为________________。(注: l—液态, g—气态)
X2(g)+2Y2O(l)。冷却后在标准状况下测得生成物的体积为 22.4 L,其密度为 1.25 g·L-1。 X2的摩尔质量为_____________, X2Y4化学式为________________。(注: l—液态, g—气态)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com