
| A、K+ 和 Na+ |
| B、CO2和NO2 |
| C、CO和CO2 |
| D、NH2- 和CH5+ |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、物质发生化学反应时不一定都伴随着能量变化 |
| B、伴有能量变化的变化都是化学变化 |
| C、在一个确定的化学反应关系中,反应物的总能量总是高于生成物的总能量 |
| D、有些吸热反应也能自发进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将苯与浓硝酸、浓硫酸的混合物在60℃水浴加热条件下反应可生成硝基苯 |
| B、用酸性高锰酸钾溶液即可检验CH2=CH-CHO中的碳碳双键 |
C、将 与NaOH的醇溶液共热制备CH3-CH═CH2 与NaOH的醇溶液共热制备CH3-CH═CH2 |
| D、淀粉在硫酸催化作用下水解,将银氨溶液加入到水解后的溶液中可检验淀粉水解的产物葡萄糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、纸上层析属于色谱分析法,其原理跟“毛细现象”相关,通常以滤纸作为惰性支持物,水作为固定相 |
| B、重结晶时,溶液冷却速度越慢得到的晶体颗粒越小 |
| C、用新制的Cu(OH)2浊液可以检验牙膏中的甘油,生成绛蓝色沉淀 |
| D、将3~4根火柴头浸于水中,片刻后取少量溶液于试管中,加AgNO3溶液和稀HNO3,可以检验火柴头中的氯元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
2- 4 |
| A、0.2 mol/L |
| B、0.25 mol/L |
| C、0.1 mol/L |
| D、0.225 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 编号 | Ⅰ | Ⅱ | Ⅲ |
| 实验 | 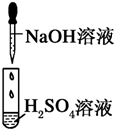 |
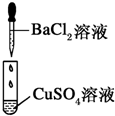 |
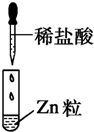 |
| 现象 | 没有明显变化,溶液仍为无色 | 有白色沉淀生成,溶液为蓝色 | 有无色气体放出 |
| A、Ⅰ中无明显变化,说明两溶液不反应 |
| B、Ⅱ中的白色沉淀为CuCl2 |
| C、Ⅲ中的离子方程式为2H++Zn═Zn2++H2↑ |
| D、Ⅲ中发生的反应不是离子反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
. |
| v |
| A、v(NH3)=0.01mol/(L?s) |
| B、v(O2)=0.03mol/(L?s) |
| C、v(NO)=0.02mol/(L?s) |
| D、v(H2O)=0.04mol/(L?s) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com