
【题目】根据要求填空:
(1)写出﹣C4H9 对应的所有结构简式
(2)丙烷的六氯代物有种
(3)一氯甲烷的电子式 ,  是甲烷的模型
是甲烷的模型
(4)某烷烃分子中同时存在﹣CH3、﹣CH2﹣、 ![]() 、
、 ![]() 四种基团,若要使烷烃碳个数最少,写出符号条件所有烷烃的结构简式
四种基团,若要使烷烃碳个数最少,写出符号条件所有烷烃的结构简式
(5)甲烷﹣氧气燃料电池,以 NaOH 做电解液,写出负极的电极反应式 .
【答案】
(1)CH3﹣CH2﹣CH2﹣CH2﹣;CH3﹣CH2(CH3)CH﹣;(CH3)2CH﹣CH2﹣;(CH3)3C﹣
(2)4
(3)![]() ;比例
;比例
(4)CH3CH2CH(CH3)C(CH3)3、CH3CH(CH3)C(CH3)2CH2CH3、CH3C(CH3)2CH2CH(CH3)2
(5)CH4﹣8e﹣+10OH﹣=CO32﹣+7H2O
【解析】解:(1)丁烷的结构简式有2种:CH3﹣CH2﹣CH2﹣CH3和(CH3)2CH﹣CH3 , CH3﹣CH2﹣CH2﹣CH3中H原子有两种,故其形成的丁基有CH3﹣CH2﹣CH2﹣CH2﹣和CH3﹣CH2(CH3)CH﹣;(CH3)2CH﹣CH3中H原子有两种,故其形成的丁基也有两种:(CH3)2CH﹣CH2﹣和(CH3)3C﹣,故丁基﹣C4H9 对应的所有结构简式有四种:CH3﹣CH2﹣CH2﹣CH2﹣;CH3﹣CH2(CH3)CH﹣;(CH3)2CH﹣CH2﹣;(CH3)3C﹣;所以答案是:CH3﹣CH2﹣CH2﹣CH2﹣;CH3﹣CH2(CH3)CH﹣;(CH3)2CH﹣CH2﹣;(CH3)3C﹣;(2)丙烷的二氯代物的异构体为:CHCl2CH2CH3 , CH3CCl2CH3 , CH2ClCHClCH3 , CH2ClCH2CH2Cl,丙烷有8个H原子,其中2个H原子被氯原子取代形成丙烷的二氯代物.六氯代物可以看作C3Cl8中的8个氯原子,其中2个氯原子被2个氢原子代替形成,两者是等效的.氯代物有四种同分异构体,可得到六氯代物也有四种同分异构体.所以答案是:4;(3)一氯甲烷的电子式为: ![]() ; 能体现物质中各原子大小比例的模型称比例模型,故
; 能体现物质中各原子大小比例的模型称比例模型,故  是甲烷的比例模型,所以答案是:
是甲烷的比例模型,所以答案是: ![]() ;比例;(4)如果某烷烃分子中同时存在这4种基团,若要使烷烃碳个数最少,则应﹣CH2﹣、
;比例;(4)如果某烷烃分子中同时存在这4种基团,若要使烷烃碳个数最少,则应﹣CH2﹣、 ![]() 和
和 ![]() 各含有一个,剩下的为甲基,设甲基的个数是x,由烷烃的通式知2(x+3)+2=2+1+3x,x=5,所以最少应含有的碳原子数是8,该烷烃的结构简式有3种,分别为CH3CH2CH(CH3)C(CH3)3、CH3CH(CH3)C(CH3)2CH2CH3、CH3C(CH3)2CH2CH(CH3)2 , 所以答案是:CH3CH2CH(CH3)C(CH3)3、CH3CH(CH3)C(CH3)2CH2CH3、CH3C(CH3)2CH2CH(CH3)2;(5)甲烷燃料电池中,负极上甲烷失电子和氢氧根离子反应生成碳酸根离子和水,电极反应式为:CH4﹣8e﹣+10OH﹣=CO32﹣+7H2O,所以答案是:CH4﹣8e﹣+10OH﹣=CO32﹣+7H2O;
各含有一个,剩下的为甲基,设甲基的个数是x,由烷烃的通式知2(x+3)+2=2+1+3x,x=5,所以最少应含有的碳原子数是8,该烷烃的结构简式有3种,分别为CH3CH2CH(CH3)C(CH3)3、CH3CH(CH3)C(CH3)2CH2CH3、CH3C(CH3)2CH2CH(CH3)2 , 所以答案是:CH3CH2CH(CH3)C(CH3)3、CH3CH(CH3)C(CH3)2CH2CH3、CH3C(CH3)2CH2CH(CH3)2;(5)甲烷燃料电池中,负极上甲烷失电子和氢氧根离子反应生成碳酸根离子和水,电极反应式为:CH4﹣8e﹣+10OH﹣=CO32﹣+7H2O,所以答案是:CH4﹣8e﹣+10OH﹣=CO32﹣+7H2O;


 学业测评一课一测系列答案
学业测评一课一测系列答案科目:高中化学 来源: 题型:
【题目】二氢荆芥内酯是有效的驱虫剂。其合成路线如下:
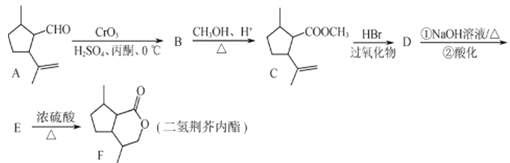
(1)A中有____个手性碳原子,B的结构简式为________。
(2)写出D在NaOH溶液中加热发生反应的化学方程式:____________。
(3)E中含氧官能团的名称是______。
(4)某物质X:①分子组成比A少2个氢原子;②分子中有4种不同化学环境的氢原子;③能与FeCl3溶液发生显色反应。写出所有符合上述条件的物质X的结构简式:__________。
(5)写出由![]() 制备
制备![]() 的合成路线图(无机试剂任选)______。合成路线流程图示例如下:
的合成路线图(无机试剂任选)______。合成路线流程图示例如下:![]()
![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH
CH3CH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】热激活电池可用作火箭、导弹的工作电源。一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为:PbSO4 +2LiCl+Ca=CaCl2+Li2SO4, 下列说法正确的是

A. 常温时,在正负极间接上电流表,指针不偏转
B. 放电过程中,Li+向负极移动
C. 正极反应式:Ca+2Cl--2e-=CaCl2
D. 每转移0.1mol电子,理论上生成20.7gPb
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我们主要从三个方面讨论一个化学反应的原理,其中不属于这三个方面的是
A. 反应进行的方向 B. 反应的快慢 C. 反应进行的限度 D. 反应物的颜色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 医用酒精的浓度通常是95%
B. 食用花生油和鸡蛋清都能发生水解反应
C. 淀粉、纤维素和油脂都属于天然高分子化合物
D. 合成纤维和光导纤维都是新型无机非金属材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有前 4 周期中的 A、B、C、D、E 五种主族元素.A 的最高价氧化物含 A 质 量分数 40%,A 原子中质子数等于中子数;B 是同周期中除稀有气体外原子半径最大的元 素;D 能形成 BD 型离子化合物,且 B、D 两离子的电子层结构相同;C 和 D 能形成 CD3 的化合物;C 原子比 E 原子多 1 个电子;B、C、D 的最高价氧化物的水化物两两均可反应 生成盐和水;D 原子比 A 原子多 1 个质子.则;
(1)B 原子结构示意图为
(2)用电子式表示 A 和 B 组成的化合物的形成过程
(3)用离子方程式表示 A 和 D 的非金属性强弱
(4)写出 C 的最高价氧化物的水化物分别和 B、D 的最高价氧化物的水化物反应的离子方 程式
(5)DE 形成的化合物中化学键类型为
(6)A2D2分子中每一个原子均达到最外层 8e﹣稳定结构,请写出其电子式和结构式、 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子组在溶液中因发生氧化还原反应而不能大量共存的是
A. H+、NO3ˉ、Fe2+、Na+ B. K+、Ba2+、OHˉ、SO42ˉ
C. Ag+、NO3ˉ、Clˉ、K+ D. Cu2+、NH4+、Brˉ、OHˉ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质分类的正确组合是
分类组合 | 纯净物 | 碱 | 盐 | 碱性氧化物 |
A | 碱石灰 | 氢氧化钡 | 苏打 | 氧化铝 |
B | H2O2 | 纯碱 | 小苏打 | 氧化镁 |
C | 水煤气 | NH3·H2O | 苛性钠 | 氧化钙 |
D | 五水硫酸铜 | 氢氧化钠 | 碱式碳酸铜 | 氧化钠 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】软锰矿的主要成分为MnO2,含少量Al2O3和SiO2。闪锌矿主要成分为ZnS,含少量FeS、CuS、CdS杂质。现以软锰矿和闪锌矿为原料制备MnO2和Zn,其简化流程如下(中间产物的固体部分已经略去)。
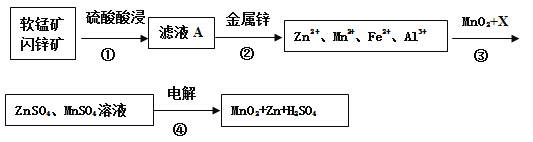
已知: Ⅰ.矿石中所有金属元素在滤液A中均以离子形式存在。
Ⅱ.各种金属离子完全沉淀的pH如下表:
Zn2+ | Mn2+ | Fe2+ | Fe3+ | Al3+ | |
pH | 8.0 | 10.1 | 9.0 | 3.2 | 4.7 |
回答下列问题:
(1)步骤①中为了加快硫酸的浸取速率,可采用的方法是_________________(任写一种)。①中发生多个反应,其中MnO2、FeS与硫酸共热时有淡黄色物质析出,溶液变为棕黄色,写出MnO2、FeS与硫酸共热发生反应的化学方程式______________________。
(2)步骤②加入金属锌是为了回收金属,回收金属的主要成分是_________。
(3)步骤③中MnO2的其作用是__________________,另外一种物质X可以是__________。
A.ZnO B.MgCO3 C.MnCO3 D.Cu(OH)2
(4)MnO2与Li构成LiMnO2,它可作为某锂离子电池的正极材料,电池反应方程式为: Li1-xMnO2+LixC6=LiMnO2+6C,写出该锂离子电池的正极电极反应式__________。
(5)已知:HCN的电离常数K=4.9×10-10,H2S的电离常数K1=1.3×10―7,K2=7.0×10―15,向NaCN溶液中通入少量的H2S气体,反应的离子方程式为__________________。在废水处理领域中常用H2S将Mn2+转化为MnS除去,向含有0.020 mol·L―1Mn2+废水中通入一定量的H2S气体,调节溶液的pH=a,当HS―浓度为1.0×10―4 mol·L―1时,Mn2+开始沉淀,则a=______。[已知:Ksp(MnS)=1.4×10―15]
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com